Infuze přípravků draslíku může být prováděna jako součást. Infuzní média
Vážení kolegové, v tomto článku bych ráda reflektovala základní principy provádění infuzní terapie (IT) v prehospitálním stadiu z pohledu resuscitátoru anesteziologa.
V kondenzované formě budeme zvažovat fyziologický základ infuzní terapie, nejběžnější infuzní média v praxi SMP, indikace pro IT a IT v některých zvláštních případech. Omlouvám se za možnou hojnost některých schémat a vzorců (snažil jsem se je co nejvíce omezit), ale podle mého hlubokého přesvědčení je to správné pochopení základů IT, které zaručuje jeho správnou implementaci.
Infuzní terapie je tedy terapie parenterální tekutinou, jejímž hlavním účelem je obnovení a udržení objemu a kvalitativního složení tekutiny ve všech vodních prostorech těla.
Trocha fyziologie a fyziky
Začněme s fyziologií metabolismu vody. Je třeba jasně pochopit, že veškerá voda lidského těla je soustředěna do několika sektorů, jejichž výměna se řídí zákony osmózy. Níže je zjednodušený diagram.
Celkový objem vody u lidí s věkem klesá (u novorozence je to 80% MT). Intracelulární tekutina je hlavní součástí protoplazmy. Extracelulární tekutina zahrnuje intravaskulární sektor (který je pro nás nejdůležitější z hlediska IT) a intersticiální sektor. Mezibuněčný sektor je také izolován (tekutina uvnitř gastrointestinálního traktu, kloubní dutiny, pleurální dutina atd.), Ale úmyslně jsem ji nezahrnul do schématu, abych jej zjednodušil. Denní potřeba vody u dospělého je v průměru 2-3 litry (při absenci jeho zvýšené spotřeby v těle - například tělesná práce). Tekutina se vylučuje normálně ledvinami (3/5 celkové odebrané tekutiny), trávicím traktem (1/5) a kůží (také 1/5). Množství moči vylučované ledvinami závisí především na objemu extracelulární tekutiny, což je důvod, proč je diuréza při resuscitaci tradičně považována za marker periferní perfúze.
Pro nás koncept jako cirkulující objem krve (bcc)což je:
u mužů - 70 ml / kg;
u žen - 60 ml / kg.
Krev teče skrz cévy (obvykle mimo větvená místa) v laminárním toku, což znamená, že se na něj vztahují všechny jeho zákony. Zejména poiseuilleův zákon, který je pro nás velmi důležitý:
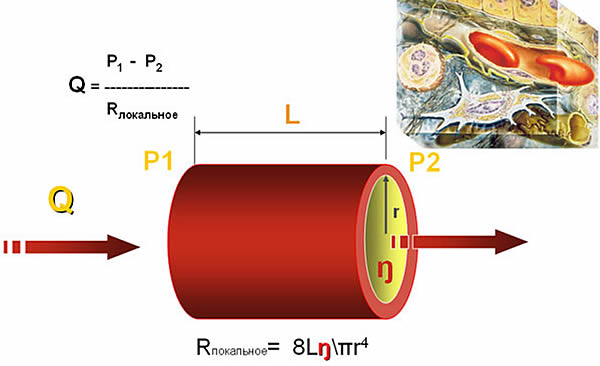
Q - tok
Z vzorce vyplývá, že hlavní hodnotou proudu je viskozita kapaliny, poloměr průřezu trubky a její délka. Všimněte si, že tlak je jen jednou z proměnných ve vzorci toku. To naznačuje, že použití samotného tlaku (BP, CVP, DZLK ...) jako indikátoru charakterizujícího perfuzi je zásadně nesprávné.
Zásadní význam pro nás má také závislost toku na průměru a délce trubky. Vezměte prosím na vědomí, že snížením průměru zkumavky dvakrát se rychlost průtoku skrz ni sníží 16krát! Zvětšení délky trubice také negativně ovlivňuje rychlost průtoku skrz ni.
Viskozita také významně přispívá k průtokům. V případě krve je hlavním ukazatelem, který zjednodušuje jeho viskozitu, hematokrit. V tomto ohledu je třeba mít na paměti, že optimální hodnota hematokritu je v tomto aspektu 0,30. Při volbě mezi krystaloidy a koloidy je třeba vzít v úvahu také viskozitu roztoků - ty mají vyšší viskozitu, a proto přetékají pomaleji, přičemž všechny ostatní věci jsou stejné.
Vybavení a cévní přístup
K dnešnímu dni jsou hlavní způsoby dodávání infuzního média do vaskulárního lože intravenózní a intraosseózní. Transfúze roztoků do tepny, nemluvě o jejich subkutánním podání, je pouze historickým zájmem. Různí výrobci vyrábějí různé systémy pro infuze, periferní a centrální žilní katétry, jehly pro intraosseózní infuze. Zvažte hlavní praktické aspekty jejich výběru.
IV Infúzní systémy . Existuje pouze jedno pravidlo - čím delší je systém, tím nižší je jeho průtok. Je možné zvýšit nádrž s roztokem nad úrovní těla, čímž se zvýší tlak a v důsledku toho i průtok, ale možnost tohoto manévrování ve stroji NSR je omezená, to by mělo být pochopeno.
Nádrže pro infuzní prostředí. Zde se vracíme k jednomu bolestivému tématu pro domácí zdravotní péči - nadále používáme řešení všude ve skleněných nádobách, což nejen zvyšuje hmotnost nádoby a zvyšuje riziko poškození, ale také zvyšuje pravděpodobnost různých reakcí spojených s tím, že se pacient dostane do krevního oběhu . lipid A, kterým jsou roztoky často při jejich přípravě kontaminovány. Řešení v plastových sáčcích jsou lehká, mobilní a velmi vhodná pro použití v praxi SMP. Díky masivnímu IT je možné přenést z těchto sáčků jejich umístěním pod tělo pacienta (samozřejmě při úplném naplnění kapátka systému, aby se zabránilo vzduchové embolii).
Katétry . Periferní katétry jsou k dispozici v různých průměrech. Plánovaná rychlost a objem infuze by měly být jasně pochopeny a průměr katétru by měl být zvolen v souladu s tím. Nezapomeňte, že rychlost infuze je určena průměrem nejužší části systému pro iv podání roztoků; obvykle je tato část katétrem. Průměr žíly a její anatomická příslušnost (periferní nebo centrální) nehraje žádnou roli v rychlosti infuze, pokud je průchodnost žíly normální. Navíc prostřednictvím centrálního venózního katétru bude kvůli jeho delší délce než periferní katétrová rychlost (se stejným průměrem katétrů) nižší. Všechny výše uvedené skutečnosti naznačují, že katetrizace centrální žíly pro „zvýšení rychlosti infuze“, pokud je to možné, pro instalaci periferního katétru velkého průměru, vypadá jako zcela neodůvodněná invazivní manipulace, která může vést k mnoha život ohrožujícím komplikacím v podmínkách DHE.
Barevné kódování periferního katétru odráží jeho průměr:
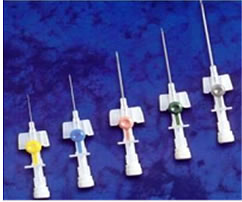
Průtok katétry různých průměrů, ml / min:
Centrální žilní katétry mají obvykle podobnou strukturu; rozsah jejich průměrů je výrazně nižší. Mohou být vyráběny samostatně nebo jako součást různých sad pro katetrizaci centrálních žil. Poslední možnost je nejpohodlnější.
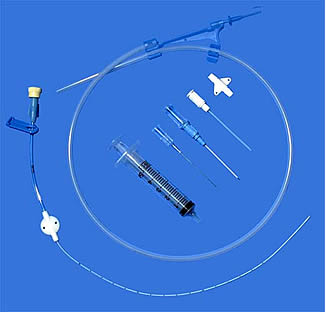
Intraosové infuzní jehly . Intraosový přístup se v poslední době stává stále populárnějším a stává se metodou volby pro pacienty s DHE, když jsou periferní žíly nepřístupné. Toto téma bylo také diskutováno na našich webových stránkách. Navzdory skutečnosti, že intraosseózní přístup lze provést běžnou jehlou s mandrinem (například silnou spinální jehlou), je pro tento účel stále výhodnější používat speciální zařízení.

Rychlost intraosseózní infuze také závisí na průměru použité jehly.
K volbě vaskulárního přístupu za podmínek DHE je třeba přistupovat velmi pečlivě. V přítomnosti normální periferní žilní sítě by měla být omezena na instalaci periferních katétrů (jeden nebo více). Absence rozvinuté podkožní žilní sítě, kdy přístup k periferním žilám buď zcela chybí nebo není dostatečný pro instalaci dostatečného počtu katetrů požadovaného průměru s absolutními indikacemi pro IT, vyžaduje intraosseózní nebo centrální žilní přístup. Vzhledem ke značnému počtu komplikací by však nemělo dojít ke katetrizaci centrálních žil v prehospitální fázi. Nezapomeňte na vnější krční žílu!
Infuzní média
Léky používané pro IT se nazývají infuzní média. Nebudeme se vyhýbat tradičnímu oddělování veškerých infuzních médií na krystaloidy a koloidy, budeme zvažovat infuzní média podle tohoto principu, ale také vyčleníme skupinu krevních náhrad se specifickým účinkem. Pochopíme, že autogenní koloidy nejsou používány v praxi SMP, budeme uvažovat pouze o syntetických drogách. Když diskutujeme o některých lécích, probereme něco jako volemický efekt - schopnost léku přitahovat vodu do vaskulárního lůžka z interstitia kvůli jeho vyšší osmolaritě, čímž se zvyšuje intravaskulární objem.
Krystaloidy. Tato skupina infuzních médií zahrnuje roztoky elektrolytů a cukrů. Nejbezpečnější léky, pokud jde o vývoj možných reakcí během transfúze a dlouhodobé následky. Jejich osmolarita a složení jsou blízké těmto indexům plazmy a extracelulární tekutiny, proto krystaloidním roztokům chybí volemický účinek. Nějaký čas po zavedení do vaskulárního lůžka jsou krystaloidy rovnoměrně rozděleny mezi intestinální a intravaskulární sektory, zatímco asi čtvrtina injikovaného objemu zůstává v intravaskulárním sektoru (viz obrázek výše). Toto je třeba vzít v úvahu při výpočtu objemu a rychlosti infuze. Toto pravidlo se nevztahuje na roztoky glukózy, ale tento problém se budeme zabývat později.
Zvažte některé z jednotlivých drog.
Izotonický
(0,85-0,9%) roztok chloridu sodného (fyziologický roztok) byl první roztok používaný k léčbě ztráty krve a dehydratace.
1 litr roztoku obsahuje: Na + - 154 mmol, C1 - 154 mmol. Celková osmolarita je 308 mosm / l, což je o něco vyšší než osmolarita v plazmě. pH 5,5 - 7,0. Používá se hlavně pro hypovolemické podmínky nejrůznějších genezí, jako dárce sodíku a chloru v případě ztráty extracelulární tekutiny. Je to výchozí řešení pro většinu podmínek vyžadujících IT. Roztok je dobře kombinován se všemi krevními náhradami. Je nemožné použít isotonické řešení jako univerzální řešení v nemocnici, protože v něm je málo volné vody, není draslík; roztok má kyselinovou reakci a zvyšuje hypokalémii, toto pravidlo však lze zanedbat v prehospitálním stadiu. Kontraindikováno v případech podezření na hypernatriémii a hyperchlorémii.
Ringerovo řešení
- isotonický roztok elektrolytu, z toho 1 litr obsahuje: Na + - 140 mmol, K + - 4 mmol, Ca2 + - 6 mmol, Cl - 150 mmol. Osmolarita 300 mosm / l. Toto řešení se používá jako náhrada krve od konce minulého století. Ringerovo řešení a jeho modifikace jsou v současné době široce využívány. Jedná se o fyziologický náhradní roztok s mírnými kyselými vlastnostmi.
Používá se k hypovolémii různé geneze, k nahrazení ztráty extracelulární tekutiny, včetně krve. Kontraindikováno v případě masivních popálenin (draslík!), Podezření na hyperchloremii a hypernatremii.
Polyionické roztoky (ionosteryl, plasmalit atd.).) mají elektrolytové složení blízké složení krevní plazmy. Optimální pro nahrazení nedostatku extracelulární tekutiny (šok, hypovolémie).
Nápravné roztoky (disol, chlorsol, acesol, soda atd.) přiřazené až po analýze iontového složení plazmy a acidobazického stavu by se proto nemělo používat v prehospitálním stadiu.
Roztoky glukózy dříve používán k doplnění bcc v hypovolémii různého původu. Jejich použití k tomuto účelu v posledních letech však bylo zcela opuštěno, protože glukóza se po krátké době po podání, která prošla všemi cykly svého metabolismu, změní na volnou vodu, která přechází do intracelulárního sektoru. V současné době je jedinou indikací pro předepisování roztoků glukózy pro DHE prokázaná hypoglykémie.
Koloidy. Z pochopitelných důvodů budeme uvažovat pouze o syntetických koloidech. Koloidní roztoky obsahují látky s vysokou molekulovou hmotností a vysokým onkotickým tlakem, což jim umožňuje přitahovat tekutinu z interstitia do vaskulárního lože (volemický efekt). Podle mého názoru je užívání drog této skupiny nejvíce odůvodněné v případě hypovolemického (traumatického, hemoragického) šoku ve 2. a 3. etapě, kdy není možné získat požadovaný objem samotnými krystaloidy kvůli jejich nedostatečnému množství (na rozdíl od nemocnice, kde může být pacient snadno transfuzován) za hodinu 3-4 litry krystaloidu se ne všechny týmy SMP mohou pochlubit přítomností takového množství roztoků). Naopak, použití samotných koloidů v prvním stádiu šoku (když je patofyziologicky pozorována dehydratace intersticiálního prostoru) je nepraktické, protože zvyšují přenos tekutiny z interstitia do vaskulárního lože. Při léčbě tohoto stádia je kompenzován intersticiální objem, takže použití krystaloidů je nejpodstatnější.
Zvažte skupinu koloidních přípravků.
Dextrans.
První koloidy, jejich analogy, se začaly používat během první světové války. Jsou to látky skládající se z glukózových polymerů s průměrnou molekulovou hmotností 40 000 (reopoliglyukin) a 70 000 (polyglyukin) D. Volemický účinek polyglukinu trvá 5–7 hodin, reopoliglyukin - 1–2 hodiny. Destrany s nízkou molekulovou hmotností (reopoliglyukin) mají výrazný disagregační účinek. Všechny dextrany jsou v CIS velmi běžné kvůli jejich nízkým nákladům a jsou stále široce používány setrvačností. Mají řadu nevýhod, které zahrnují především negativní účinek na hemokoagulační systém (provokují a zvyšují fibrinolýzu, inaktivují šestý faktor). Nezapomeňte také na negativní účinky těchto léků na renální parenchym („dextran burn“). Dextrany v těle jsou metabolizovány velmi pomalu a hromadí se v retikulo-histiocytickém systému. Alergické reakce (včetně fatálních) jsou během transfúze dextranů zcela běžné a vědci hodnotí riziko fatální alergické reakce na dextrany i riziko úmrtí na akutní apendicitidu.
Indikace:deficience intravaskulárního objemu (akutní hypovolémie). Reopoliglyukin se také používá při poruchách mikrocirkulace různého původu.
Maximální denní dávka dextránových přípravků je 1000 ml.
Příprava:polyglucin, reopoliglukin, makrodex, reomacrodex atd.
Želatina a její analogy.
Nalezené a široce používané. Obsahují peptidy s různou molekulovou hmotností. Volemický účinek je nižší než účinek dextranů a trvá pouze několik hodin. Dříve se věřilo, že želatinové přípravky neovlivnily koagulační systém, ale ukázalo se, že to nebylo daleko od případu. Želatina zvyšuje čas krvácení, zhoršuje tvorbu sraženin a agregaci destiček. Zajímavá situace také nastala v souvislosti s hrozbou šíření původce přenosné spongioformní encefalopatie (krávy vztekliny) prostřednictvím želatinových přípravků, které nejsou ničeny běžnými sterilizačními režimy.
Kombinované použití přípravků dextrán a želatina vede k rozvoji krvácení, protože jejich negativní účinek na koagulační systém se vzájemně zvyšuje.
Indikace: akutní hypovolémie.
Želatinové přípravky jsou nežádoucí pro použití v pozdním těhotenství - při použití jsou zaznamenány endoteliální léze, zvýšení propustnosti, zvýšení uvolňování histaminu se všemi následnými důsledky.
Příprava:želatina, hemogel, MPF.
Hydroxyethylškrob (HES) přípravky.
Relativně nová skupina koloidních krevních náhrad pocházejících z amylopektinového škrobu (přírodní polysacharid). Molekula HES sestává z polymerovaných zbytků glukózy. Přípravky HES poskytují výrazný volemický účinek, jehož trvání závisí na molekulové hmotnosti léčiva a stupni substituce. HES jsou netoxické, nemají výrazný negativní účinek na koagulaci krve (ačkoli by jejich dávka měla být během hypokoagulace snížena) a zřídka způsobují závažné alergické reakce.
Indikace:akutní hypovolémie.
HES přípravky zahrnují: Reftan, Stabizol, HAES-Steril, Vololek atd.
Krevní náhražky se specifickým účinkem. Zde se dotknu jednotlivých drog, které nějak našly svou aplikaci na DHE.
Osmodiuretika.
Hlavní indikací pro jmenování do DHE je mozkový edém. Obvykle se používá mannitol - hyperosmolární roztok mannitol hexatomického alkoholu, který stimuluje diurézu. V těle není metabolizován a vylučován ledvinami.
Kontraindikovanés dekompenzovaným selháním ledvin, akutním srdečním selháním, šokem.
Jedna dávka 20% roztoku je 200 až 400 ml. Představeno na 30-60 minut.
Koloidy s detoxikačním účinkem. Zastaralá skupina léčiv na bázi polyvinylpyrrolidonu a polyvinylalkoholu. Typičtí představitelé: hemodéza, neohemodéza, polydéza. Poskytují mnoho vedlejších účinků, počínaje těžkými pyrogenními reakcemi a končící porážkou parenchymálních orgánů. V současné době se jejich používání důrazně nedoporučuje.
Algoritmus pro praktické zavedení infuzní terapie na DHE
- Určete indikace pro infuzi. Infuzní terapie DHE, stejně jako jakékoli jiné terapeutické činidlo, by se mělo používat pouze pro přísné indikace. Kapání babiček mildronátem na jejich žádost není součástí úkolů NSR.
- Určete umístění IT (na místě, během přepravy).
- Stanovte objem infuzní terapie a její kvalitativní složení v závislosti na dostupných lécích a jejich množství.
- Určete potřebnou rychlost infuze. Jeden mililitr krystaloidního roztoku obsahuje v průměru 20 kapek.
- V souladu s určitým objemem a rychlostí řešit problém cévního přístupu (periferie, centrální, jeden nebo více). Nikdy se neomezujte na jeden katétr (i velký průměr) v případě nárazu - existuje riziko ztráty žíly během přepravy.
- Provést cévní přístup (jeden nebo více), věnujte velkou pozornost fixaci katétru.
- Zahajte infuzní terapii.
- V procesu infuze jasně představují:
- rychlost infuze;
- transfuzovaný objem;
- dynamika stavu pacienta,
oprava v souladu se všemi těmito terapeutickými opatřeními.
9. Při dodání pacienta do nemocnice poskytněte lékaři, který ho vezme, informace o tom, kolik, co a jakou rychlostí byl pacient transfuzován. Všechny tyto informace odrážejte na volací kartě a na krycím listu.
Provádění infuzní terapie ve vybraných klinických situacích
Hypovolemický (hemoragický, traumatický) šok.
Infuzní terapie je hlavní léčba hypovolemického šoku. Všechna další opatření (imobilizace, analgezie, specifická terapie) mají druhořadý význam a provádějí se pouze na pozadí odpovídající infuze. Častou chybou je předepsat léky proti bolesti v šoku bez podpory hemodynamické infuze, což často vede ke katastrofickému kolapsu posledně jmenovaného.
Pro orientaci z hlediska objemu a rychlosti infuze v případě hypovolemického šoku mě nejvíce zaujalo schéma Americké vysoké školy chirurgů, ve kterém je výpočet objemu IT založen na nedostatku BCC. V souladu s tímto schématem se rozlišují čtyři třídy hypovolemie:
Ztráta krve méně než 10% BCC (méně než 500 ml) nevyžaduje léčbu, je asymptomatická.
KlinikaStupeň 1 - klinika může chybět nebo existuje ortostatická tachykardie. V intersticiálním sektoru je nedostatek tekutin.
Stupeň 2 - ortostatická hypotenze, úzkost, mírná inhibice.
Stupeň 3 - arteriální hypotenze ve vodorovné poloze, oligurie, omračování.
4. stupeň - těžká hypotenze, anurie, stupor a kóma.
Vždy si to pamatujte objem ztráta krve je velmi důležitá rychlost poslední. Blesková krevní ztráta 50% BCC může vést k okamžité smrti pacienta v důsledku vývoje syndromu „prázdné srdce“. Současně je pacientům dostatečně dobře tolerována dostatečně velká krevní ztráta, která se v průběhu času natahuje.
Deficit bcc se předběžně vypočítá podle výše uvedené tabulky.
Objemové doplňování se provádí preparáty krystaloidů a koloidů. Při kompenzaci nedostatku bcc krystaloidními přípravky by měl být jejich objem 3-4krát větší než odhadovaný deficit bcc. Při použití koloidů by jejich objem měl být roven dvěma třetinám nebo celkovým deficitům bcc. V praxi se používá kombinované použití koloidních a krystaloidních přípravků v poměru 1: 1, 1: 2, 1: 3.
V tabulce je uveden indikativní systém kompenzace v závislosti na třídě hypovolémie a deficienci BCC.
Poznámka k tabulce. Je zřejmé, že v případě absence krevních produktů není třeba hovořit o úplné kompenzaci ztráty krve stupně 3 a 4 na DHE, úkolem personálu NSR je však co nejvíce stabilizovat pacienta dostupnými řešeními.
Infuzní terapie s nízkým objemem
v posledních letech získala distribuci právě mezi pracovníky zdravotnických služeb katastrof. A to je pochopitelné, protože právě pre-nemocniční pracovníci byli vždy problémem a rychlostí kompenzace. Podstatou maloobjemové infuzní terapie je použití hypertonického roztoku chloridu sodného, \u200b\u200bkterý prudkým zvýšením osmolarity plazmy vtahuje vodu do krevního řečiště, čímž pomáhá získat čas. Použití hypertonického roztoku chloridu sodného v případě hypovolemického šoku, jak v experimentu, tak na klinice, ukázalo jeho nepochybné výhody.
Současně se používají heterogenní koloidní roztoky (10% roztok dextran-60-70 nebo hydroxyethylškrob), které zvyšují onkotický tlak plazmy a mají tedy hemodynamický účinek. Současné použití hypertonického roztoku chloridu sodného a koloidů se projevuje kombinovaným účinkem spojeným se zvýšením osmolarity plazmy a onkotickým tlakem. Účelem použití koloidů v této kombinaci je udržení kompenzovaného intravaskulárního objemu po dlouhou dobu.
Hlavní účinky pozorované při zavedení hypertonického roztoku chloridu sodného v HS:
rychle zvyšuje srdeční výdej ADi;
zvyšuje účinnou perfuzi tkání;
snižuje riziko opožděného selhání více orgánů.
Zároveň bychom neměli zapomenout na nebezpečí používání solných roztoků. Možné nebezpečí jejich použití zahrnuje vývoj hyperosmolárního stavu, negativní inotropní účinek (v důsledku rychlé infuze), zvýšené ztráty krve v případě nezastavitelného krvácení.
Hlavním rozdílem této metody je „nízkoobjemový princip“, tj. celkový objem kompenzace tekutin za ztrátu krve by měl být mnohonásobně menší než při použití roztoků isotonického krystaloidu.
Technika malé infuze:
celkový objem injikovaného hypertonického roztoku chloridu sodného by měl být 4 ml / kg tělesné hmotnosti, tj. od 100 do 400 ml;
roztok se podává ve frakčních bolusových dávkách 50 ml s krátkými přestávkami (10-20 minut);
zavedení fyziologického roztoku je kombinováno s 10% roztokem dextran-60-70 nebo s přípravky HES;
zavádění roztoků je zastaveno normalizací krevního tlaku, stabilní hemodynamikou a dalšími známkami absence šoku.
Kritéria pro účinnost infuzní terapie pro hypovolemický šok:
- Zvýšení a stabilizace systolického krevního tlaku nad 100 mm Hg. Art.
- Snížení srdeční frekvence pod 100 tepů / min.
- Obnovení vědomí (známka adekvátní perfuze mozku).
- Zlepšení mikrocirkulace (barva a teplota pokožky).
Pokud má pacient s hypovolemickým šokem nedostatečnost myokardu (příznaky mohou být dušnost, vlhké srážky v dolních plicích na pozadí masivní infuze), je nutná inotropní podpora (dopamin). Zvláště chci zdůraznit, že zavedení inotropních a vasivních léků se provádí až po alespoň částečné kompenzaci BCC.
Dehydratace různého původu. Nejčastěji se člověk musí vypořádat s isotonickou dehydratací (ztráta vody a solí ve stejném množství) se střevními infekcemi, nezvratným zvracením, průjmem a horečkou. Zpravidla nevyžadují rychlou infuzi velkého objemu. K vyrovnání nedostatku tekutin se obvykle používají krystaloidní roztoky v počáteční dávce 10 ml / kg tělesné hmotnosti pacienta. Koloidní přípravky v kombinaci s krystaloidy se používají pouze se zřetelnými příznaky dehydratačního šoku (významná hypotenze, tachykardie, zhoršené vědomí).
Anafylaktický šok vyžaduje rychlou infuzi krystaloidních přípravků v kombinaci s použitím adrenalinu. Obvykle nalijte trysku 2500 - 4000 ml izotonické řešení chlorid sodný. V kombinaci se zastavením úniku kapilár, který způsobuje adrenalin, infuzní terapie pomáhá naplnit cévní lůžko a stabilizovat hemodynamiku.
Popáleniny. Těžké popáleniny jsou doprovázeny závažnou hypovolémií spojenou s únikem tekutin z krevních cév do interstitia v důsledku obecného zvýšení propustnosti kapilár, odpařování vody z povrchu hoření a redistribuce tekutiny do oblasti poškození. Nedostatečné IT je jednou z nejčastějších příčin úmrtnosti pacientů s popáleninami. Infuze by měla začít v prehospitální fázi a pokračovat v nemocničním prostředí. První den se k infuzi používají pouze krystaloidové roztoky, protože v důsledku zvýšeného úniku kapilár vede použití koloidů k \u200b\u200bjejich vstupu do interstitia s následným vývojem významného edému. Při zavádění roztoků polyiontových krystalů obsahujících draslík je třeba věnovat zvýšenou pozornost jeho obsahu v plazmě pacientů s popáleninami, zejména při absenci dostatečné diurézy, což může rychle vést k hyperkalémii. Pro výpočet objemu infuze popálenin se v současnosti považuje Parklandova formulace za obecně přijímanou:
V infuze \u003d 4 x MT x% hoření
kde MT je tělesná hmotnost pacienta.
Objem se počítá první den a polovina z něj se nalije během prvních šesti hodin. V souladu s tím staví infuzní program v prehospitální fázi.
Příklad výpočtu: pacient vážící 70 kg, spálená plocha 25% povrchu těla. Výpočet: 4 x 70 x 25 \u003d 7000 ml. Polovina tohoto objemu musí být transfuzována za 6 hodin - 3500 ml. Proto musí pacient v první hodině nalít 600 ml zaoblené.
Anestezie a další opatření u pacienta s popáleninami se provádí až po zahájení infuzní terapie.
Traumatické poškození mozku. Při nepřítomnosti hypovolémie je infúze v TBI omezena pouze denním požadavkem pacienta na tekutinu. Optimálním výchozím řešením pro jeho implementaci je isotonický roztok chloridu sodného. Infuze začíná pomalu se zaměřením na hemodynamické parametry a neurologický stav pacienta. Nucené zavádění tekutiny může vést ke zvýšení mozkového edému se všemi následnými následky; současně není nestabilní hemodynamika u pacienta s poraněním hlavy o nic méně nebezpečná. Systolický krevní tlak by měl být udržován v rozmezí 120 - 150 mm RT. Čl., Přičemž se zabrání přetížení vodou a v případě potřeby se používá vazopresorová léčiva.
Pacienti se srdeční patologií obvykle velmi špatně tolerují objemové zatížení (pokud nemají počáteční hypovolémii). Výjimkou v kardiologii, která vyžaduje aktivní infuzní terapii, je infarkt myokardu pravé komory. V tomto případě lze udržovat dostatečný srdeční výdej pouze pomocí infuze. Ve všech ostatních případech by mělo být zavádění tekutiny pacientovi se srdeční patologií co nejmenší. Všechna léčiva vyžadující infuzi (nitroglycerin, dopamin atd.) Se ředí v minimálním množství rozpouštědla. Infuzní terapie u těchto pacientů se provádí velmi pečlivě, se zaměřením na celkový stav, hemodynamické parametry a auskultační obraz v plicích.
Ketoacidotické a hyperosmolární koma u diabetes mellitus. Infuzní terapie v tomto stavu v prehospitálním stádiu je omezena na infuzi isotonického roztoku chloridu sodného rychlostí 15-20 ml / min a infuze pokračuje během přepravy. Celkový objem infuze by měl být 500–1 000 ml u dospělých a 10 ml / kg u dětí. Nemůžete vstoupit sodu, roztoky obsahující draslík a inzulín.
Časté chyby během infuzní terapie
- Nedostatečný objem a rychlost infuze. Často se vyskytuje v léčbě hypovolemického šoku. Vede to k neúčinnosti infúze, další destabilizaci hemodynamiky a zhoršení dysfunkce více orgánů. Vždy byste měli instalovat tolik katétrů, kolik je nezbytných pro dostatečnou infuzi!
- Příliš aktivní a objemná infuze. Před zahájením IT byste měli vždy vyhodnotit stav kardiovaskulárního systému pacienta na přítomnost nedostatečnosti myokardu. Nadměrná infuze je zvláště nebezpečná u malých dětí, které je vždy lepší mírně zkrátit než přeplnit. Objemové přetížení vede ke zvýšení selhání levé komory až do rozvoje plicního edému. Nikdy nezapomenete na známou aforismus resuscitátorů, že infuzní terapií se utopilo více lidí, než se utopili v kanálu La Manche.
Klinický případ.Pacient M., 47 let, byl na JIP pro těžké doprovodné zranění. Pacient podstoupil mechanickou ventilaci. Resuscitační lékař ve službě, věnující pozornost nízkému CVP (0 cm vodní sloupec) a určité hypotenzi (krevní tlak 100/60 mmHg), se rozhodl zvýšit objem infuzní terapie, a to i přesto, že pacient měl dostatek diurézy. . Lékař podal infuzi 2 000 ml krystaloidních roztoků za 1 hodinu, ale poté, co obdržel pouze malé zvýšení CVP (2 cm vody, art.), Převedl v průběhu další hodiny pacientovi dalších 2000 ml krystaloidu. Pacientův stav se prudce zhoršil, objevil se obraz akutního selhání levé komory následovaný plicním edémem. Plicní edém byl zastaven, pacient byl o den později odstraněn z mechanické ventilace, další průběh nemoci bez rysů, s uzdravením.
Chybou lékaře byla orientace na jeden indikátor - CVP a ignorování dalších známek adekvátní perfuze tkání, což vedlo k naprosto nepřiměřenému jmenování infuze.
- Odmítnutí inotropní podpory během vývoje příznaků srdečního selhání u pacienta během masivní infuzní terapie také vede k rozvoji akutního selhání levé komory.
- Použití inotropů až do alespoň částečného doplnění BCC vede ke zhoršení centralizace krevního oběhu, zhoršení krevního oběhu orgánů a rozvoji selhání více orgánů. Nejprve jsou postiženy játra a ledviny.
- Jmenování roztoků glukózy pro infuzi vede k rozvoji intracelulárního edému a nedostatečnému hemodynamickému účinku infuze, protože roztoky glukózy rychle opouštějí cévní lože.
- Jmenování koloidních roztoků pro dehydratační syndrom (pokud není šok) vede k dalšímu zhoršení dehydratace intersticiálního sektoru.
- Jmenování některých koloidů při doplňování BCC při hypovolemickém šoku také vede k dehydrataci intersticiálního prostoru.
Na závěr bych rád zdůraznil, že infuzní terapie je silnou zbraní v rukou odborníka s kompetentním a včasným použitím a často určuje další výsledek onemocnění. Jeho opuštění v prehospitální fázi v těch případech, kdy je to nutné, tedy vypadá zcela neodůvodněné a trestněprávní. Nikdy se nesnažte kapat "okem", je plná jak nedostatečné, tak i nadměrné infuze. Během infuzní terapie vždy vyhodnoťte a analyzujte stav pacienta.
Shvets A.A. (Počet)
Infuzní média jsou léky používané pro parenterální tekutinovou terapii.
Všechna infuzní média nebo roztoky, v závislosti na vlastnostech a účelu, jsou rozděleny do následujících skupin:
1) koloidní infuzní roztoky - heterogenní a autogenní (roztoky dextranu, želatiny, škrobu, krevních produktů a krve);
2) krystaloidní infuzní roztoky - roztoky elektrolytů a cukrů;
3) detoxikační roztoky - specifická skupina koloidů s nízkou molekulovou hmotností s detoxikačními vlastnostmi;
4) roztoky s multifunkčním účinkem;
5) krevní náhražky s funkcí transportu plynu - roztoky schopné vykonávat funkci transportu kyslíku a oxidu uhličitého bez účasti červených krvinek;
6) přípravky pro parenterální výživu.
ŘEŠENÍ INFUZE KOLOIDŮ
HETEROGENNÍ koloidní řešení
Dextran Dextran je produkován mikroby na médiu obsahujícím cukr a je ve vodě rozpustný vysokomolekulární glukózový polymer. V roce 1943 byla hydrolýzou nativního dextranu získána makrodexová frakce, jejíž vodné roztoky měly podobné vlastnosti jako krevní plazma. Dextran se rychle rozšířil do celého světa a již v roce 1953 v SSSR bylo získáno řešení dextranu, zvaného polyglucin.
Polyglukina. Polyglukin - 6% roztok dextranu s průměrným mol. o hmotnosti 50 000 až 70 000. Obsahuje dextrán o střední molekulové hmotnosti (6 g), chlorid sodný (9 g), ethylalkohol (0,3%), vodu pro injekce (do 1000 ml). Relativní viskozita 2,8-4; KÓD - 58 mmHg, pH 4,5-6,5; osmolarita - 308 mosm / l. Cizí analogy - makrodex, intradex, infukol atd. Mají průměrný mol. hmotnost od 60 000 do 85 000.
Vysoká molekulová hmotnost a vysoká CHSK polyglucinu zajišťují jeho retenci v krevních cévách a zvýšení CPP. Molekuly polyglucinu jsou dlouhodobě zadržovány ve vaskulárním loži a mají výrazný hemodynamický účinek. Při šoku mají středomolekulární dextrany pozitivní účinek na krevní oběh po dobu 5 až 7 hodin a při nedostatku krve do 1 litru lze polyglucin nebo makrodex použít jako jediný prostředek k léčbě hypovolémie. Frakce polyglucinu s nízkou molekulovou hmotností má pozitivní vliv na reologické vlastnosti krve a zlepšuje mikrocirkulaci.
Ihned po infuzi polyglucin začíná opouštět cévní lože. Během prvního dne se jeho hlavní hmota vylučuje v nezměněné podobě močí.
Polyglukin je indikován ve všech případech akutní hypovolémie. Jedna dávka od 400 do 1000 ml nebo více. Dávka a rychlost podávání závisí na konkrétní situaci. Maximální dávka dextrans 60-85 je 1,5-2 g / kg za den. Překročení této dávky může být doprovázeno krvácením. Přestože jsou roztoky polyglucinu netoxické a nepyrogenní, jejich podávání může být doprovázeno alergickými a anafylaktickými reakcemi. Aby se jim zabránilo, měl by být proveden stejný biologický test jako při zavedení plné krve. Za stejným účelem lze monovalentní dextrán 1 (Fresenius) použít v dávce 20 ml po dobu 2 minut. Nejdůležitější podmínkou prevence je vytvoření dextranů s úzkým zaměřením, které neobsahují frakce s vysokou molekulovou hmotností.
Stejná skupina léků zahrnuje polyphere (blízký analog polyglucinu, který je určen k léčbě hypovolemických stavů a \u200b\u200bstimulace hematopoézy), rondex (má zlepšené funkční vlastnosti ve srovnání s polyglucinem, jeho relativní viskozita nepřesahuje 2,8; normalizuje centrální hemodynamiku, zlepšuje periferní krevní oběh) a inhibuje adhezivní vlastnosti destiček), polyglyusol (vytvořený na základě roztoku polyelektrolytu).
Všechna středomolekulární roztoky dextranu mají hlavně funkci nahrazující objem a působí na centrální hemodynamiku. Akutní ztráta krve nebo plazmy je však také doprovázena narušenou periferní cirkulací, která vyžaduje korekci reologických charakteristik krve. Dextrany s nízkou molekulovou hmotností se označují jako reologické přípravky.
Reopoliglyukin. Reopoliglyukin - 10% koloidní roztok dextránu s průměrným molem. o hmotnosti 30 000 až 40 000. Obsahuje dextrán s nízkou molekulovou hmotností (100 g), chlorid sodný (9 g), glukózu (60 g), vodu pro injekce do 1000 ml. Relativní viskozita - 4-5,5; pH 4-6,5. Osmolarita léčiva v 0,9% roztoku chloridu sodného je 308 mosm / la 667 mosm / l, pokud je léčivo v 0,9% roztoku chloridu sodného s glukózou.
Dextrans s molo. o hmotnosti 40 000 a méně patří do skupiny dextranů s nízkou molekulovou hmotností. Poskytují největší, ale krátkodobý efekt. Díky své vysoké koncentraci mají dextrany s nízkou molekulovou hmotností rychlý a silný účinek expandéru. Síla vazby vody překračuje fyziologickou sílu vazby na krevní proteiny, což vede k pohybu tekutiny z intersticiálního sektoru do cév, 1 g reopoliglukinu váže 20-25 ml vody. Zvýšení plazmatického objemu při použití dextranu 40 je nejvýraznější během prvních 90 minut po podání. Rolemický koeficient reopoliglyukina asi 1,4. 6 hodin po infuzi se obsah reopoliglyukinu v krvi sníží asi 2krát, až 80% léčiva se vylučuje v první den močí. Reopoliglyukin má výrazný disagregační účinek na krevní destičky. Tvoří molekulární vrstvu na povrchu krevních buněk, buněčných membrán a vaskulárního endotelu, což snižuje riziko intravaskulární koagulace a rozvoje DIC. Negativní stránkou této akce je možnost krvácení. Nebezpečí takové komplikace se zvyšuje s jmenováním velkých dávek nízkomolekulárních a středomolekulárních dextranů (více než 1,5 litru pro dospělé).
Indikace pro jmenování reopoliglukinu: poruchy mikrocirkulace, bez ohledu na etiologii (šok, popálení v akutním období, sepse atd.), Tendence k hyperkoagulaci a trombóze.
Anafylaktoidní reakce a další komplikace infekce reopolyglucinu jsou vzácné a obvykle se snadno vyřeší „standardní“ terapií.
Cizí analogy reopolyglucinu: reomacrodex, longasteril-40, reofuzin, reodex a další se liší od domácího složení solí a užšího molekulárního rozdělení frakcí.
Želatina Želatina je vysokomolekulární ve vodě rozpustná látka živočišného původu, která není úplným proteinem. Na rozdíl od jiných proteinů nemá specifičnost, a proto se používá jako náhrada krve.
Želatina. Želatina - 8% roztok částečně hydrolyzované jedlé želatiny. Obsahuje peptidy různých molekulových hmotností. Průměrný mol. jeho hmotnost je 20 000. Relativní viskozita 2,4 - 3,5; hustota 1 035; CODE 220-290 mm vodní kolona; pH 6,7 - 7,2.
Mechanismus účinku gelatinolu je způsoben jeho koloidními vlastnostmi. Síla vázání vody v želatinových roztocích je menší než síla dextranů, působení expandéru není charakteristické. Aktivní akce trvá jen několik hodin. Po 24 hodinách zůstávají v krvi pouze stopy želatiny. Želatinové roztoky mají nižší kapacitu nahrazující objem než dextrán, volemický koeficient 0,5. Rychleji se distribuují v extracelulárním prostoru, což je činí méně nebezpečnými z hlediska možnosti přetížení srdce. Se zavedením gelatinolu dochází k hemodilučnímu efektu bez narušení koagulace krve. Zavádění želatiny je indikováno pro hypovolémii, a to iu pacientů s poruchami srážení krve. Částečně štěpená želatina se vylučuje téměř celé ledvinami. Se zavedením želatiny se vyvíjí polyurie s relativně nízkou hustotou moči a zrychluje se vylučování toxických metabolitů. Předpokladem pro realizaci tohoto detoxikačního účinku je dostatečná vylučovací funkce ledvin. Část zavedeného gelatinolu je schopna rozložit se a vytvořit malé množství energie.
Cizí analogy: plasmagel, hemogel, neoplasmazhel, fyziogel; Helifundol, hemacel, modifikovaná kapalná želatina (IFF) atd.
Škrob. V posledních letech se hojně vyskytují krevní náhrady rostlinného původu založené na ethoxylovaném škrobu částečnou hydrolýzou kukuřičného škrobu. Tato léčiva jsou netoxická, nemají negativní účinek na koagulaci krve a nezpůsobují alergické reakce. Mají úzkou strukturální afinitu k glykogenu, což vysvětluje vysokou toleranci hydroxyethylškrobu v těle. Je schopen se rozložit s uvolněním nesubstituované glukózy. Na rozdíl od dextranů je molekulová hmotnost hydroxyethylškrobu mnohem vyšší, ale to není významné při hodnocení jeho vlastností. Ve svém hemodynamickém a protišokovém působení jsou škrobové roztoky podobné dextranům. Trvání oběhu a volemické vlastnosti hydroxyethylškrobu závisí na molekulové hmotnosti a stupni substituce. Takže se stupněm substituce 0,7 každých 10 jednotek. glukóza obsahuje 7 hydroxyethylových skupin. Při stupni substituce 0,7 je poločas vysazení léčiva až 2 dny 0,6 - 10 hodin a 0,4 - 0,55 - ještě méně. Koloidní účinek 6% hydroxyethylškrobu je podobný lidskému albuminu. Po infuzi 1 litru plazmasterilu (mol. Hmotnost 450 000, stupeň substituce 0,7) trvá zvýšení plazmatického objemu déle než 6 až 8 hodin. Infúze roztoků škrobu, zejména plasmasterilu, přispívá ke snížení systémové a pulmonální periferní vaskulární rezistence. Na rozdíl od heterogenních koloidních roztoků a jako lidský albumin, 6% hydroxyethyl škrob velmi mírně zvyšuje průměrný plicní tlak, zatímco poskytuje významné zvýšení systolického objemu srdce. Plasmasteril způsobuje mírné zpomalení koagulace krve v rámci fyziologických parametrů a působí proti pooperační patologické hyperkoagulaci. Infuze Plasmasterilu způsobují aktivaci renálních funkcí a stimulují diurézu.
V současnosti vyvinuté a široce používané, zejména v zahraničí, roztoky (3%, 6%, 10%) hydroxyethylového škrobu o střední molekulové hmotnosti s mol. hmotnost 200 000 a stupeň substituce 0,5. Snížit mol. hmotnost a stupeň substituce snižuje dobu oběhu roztoku v plazmě. Zvýšení koloidní koncentrace zvyšuje počáteční účinek objemu. Vzhledem k průměrné molekulové povaze koloidu se člověk nemůže obávat významného hyperonkotického účinku. Díky specifickým reologickým a antitrombotickým vlastnostem mají tato média pozitivní účinek na mikrocirkulaci, normalizují koagulaci destiček a plazmy, aniž by zvyšovaly riziko krvácení. To vše nám umožňuje doporučit hydroxyethylškrobové přípravky pro široké použití nejen k prevenci a léčbě deficitu objemu a šoku, ale také k prevenci tromboembólie a léčbě poruch periferního oběhu.
Wolekam - domácí drogana bázi ethoxylovaného škrobu. Jeho molo. hmotnost 170 000 a stupeň substituce 0,55-0,7. Podle vlastností je to blízko k japonské drogě.
Plasmasteryl ("Frezenius") - 6% hydroxyethylškrob, mol. hmotnost 450 000, stupeň substituce 0,7.
HAES-steril ("Fresenius") - roztok hydroxyethylového škrobu o střední molekulové hmotnosti. Jako hmotnost 200 000, stupeň substituce 0,5.
AUTOGENNÍ KOLIDNÍ ŘEŠENÍ
Autogenní koloidní roztoky zahrnují plazmu, albumin, protein a krev.
Krevní plazma obsahuje 90% vody, 7-8% bílkovin, 1,1% neproteinových organických látek a 0,9% anorganických látek. Převážná část plazmy je albumin.
Nativní plazma. Navzdory všem indikacím je použití nativní plazmy omezeno krátkou skladovatelností (až do dne), možností infekce viry hepatitidy B a AIDS.
Čerstvě zmrazená plazma má oproti nativní plazmě několik výhod. Může být skladován při -30 ° C po dobu jednoho roku v uzavřených obalech. Je bez plazmových deficiencí a obsahuje prakticky všechny faktory hemostatického systému.
Indikace pro použití čerstvě zmrazené plazmy jsou masivní ztráta krve a plazmy, všechna stádia onemocnění popálením, hnisavé septické procesy, těžké trauma, kompresní syndrom s rizikem vzniku akutního selhání ledvin. Je to droga volby pro DIC. Transfuze čerstvě zmrazené plazmy je indikována pro koagulopatie s nedostatkem koagulačních faktorů II, V, VII, XIII, s heparinovou terapií při léčbě trombózy. Použití velkých objemů čerstvě zmrazené plazmy je nedílnou součástí intenzivní péče o těžké trauma, kompresní syndrom. Ve srovnání s jinými autologními koloidními roztoky je čerstvě zmrazená plazma nejvíce spotřebovanou složkou při pohotovostní lékařské péči uprostřed přírodních katastrof.
Vstup do krve aktivátorů srážení krve ze zničených tkání je skutečnou hrozbou pro rozvoj akutního selhání ledvin. V těchto případech je ukázáno, že je možné včasné použití čerstvě zmrazené plazmy, což je nosným faktorem antikoagulačního systému, přírodních protidestičkových látek a plasminogenu. Čerstvě zmrazená plazma je vysoce účinné koloidní médium hemodynamického působení. Tato krevní složka nejvíce kompenzuje ztrátu různých typů proteinů. Může být použit během terapeutické plazmaferézy.
Dávka infúzní plazmy je stanovena patologií a pohybuje se v rozmezí od 100 ml do 2 litrů denně nebo více [Zhizhevsky Y.A., 1994]. Před transfuzí se čerstvě zmrazená plazma rozmrazí ve vodní lázni při teplotě 35 - 37 ° C. Měl by být průhledný, slámově žluté barvy, bez zákalu, vloček a vláken fibrinu. Mělo by být okamžitě transfukováno. Rychlost vstřikování je od kapání po inkoustovou. Měla by to být jedna skupina s krví pacienta. Vyžaduje se biologický test: trysková infuze prvních 10 až 15 ml plazmy, která sleduje pacienta po dobu 3 minut; při absenci změn stavu pacienta - opakovaná trysková infuze 10 - 15 ml plazmy a pozorování po dobu 3 minut: pokud nedochází k žádné reakci, provede se vzorek potřetí. Pokud pacient nereagoval na žádný ze vzorků subjektivně ani objektivně, pak je vzorek považován za negativní a v krevní transfuzi lze pokračovat. Kontraindikace při jmenování plazmatických roztoků je senzibilizace pacienta k parenterálnímu podávání proteinu.
Koncentrovaná nativní plazma má výraznější hemostatické vlastnosti. Průměrná dávka pro krvácení je 5-10 ml / kg / den; s nedostatkem proteinu - 125-150 ml / den s 2-3denními přestávkami.
Antistafylokoková lidská plazma se používá k léčbě purulentně-septických komplikací způsobených kokainovou patogenní flórou.
Albumin je frakcionovaný přípravek lidské plazmy. K dispozici v lahvích v 5%, 10% a 20% roztoku.
Krevní albumin je hlavním cirkulujícím jemně rozděleným proteinem. Jeho molo. hmotnost 68 000 - 70 000. Albumin udržuje vysoký CODE v krvi a pomáhá přitahovat a zadržovat tkáňovou tekutinu ve vaskulárním loži. Podle osmotického tlaku odpovídá 1 g albuminu 18 ml tekuté plazmy, 25 g albuminu 500 ml plazmy.
Albumin se podílí na výměně krve a tkání, je rezervou proteinové výživy a univerzálním prostředkem pro transport enzymů, hormonů, toxinů a drog. Hraje hlavní roli při udržování CHSK v plazmě, a proto je obzvláště nezbytné ke snížení objemu plazmy způsobeného hypoalbuminemií; 5% roztok albuminu poskytuje stejný onkotický tlak jako plazma. Čím vyšší je koncentrace roztoku, tím větší je jeho účinek nahrazující objem. Účinek 100 ml 20% roztoku albuminu přibližně odpovídá účinku 400 ml plazmy. S dehydratací musí být zavedení 10% a 20% roztoku albuminu spojeno se zavedením 2-3násobných objemů krystalických roztoků.
Indikace pro jmenování roztoků albuminu: akutní ztráta krve a plazmy, snížený objem plazmy, katabolismus bílkovin a zejména hypoalbuminemie. Rychlost podávání se pohybuje od velmi pomalé rychlosti infuze po tryskové podání. Při mírné hypoalbuminemii je celková denní dávka 100-200 ml 5% nebo 10% roztoku. S výraznější ztrátou proteinů a hypovolémií lze denní dávku zvýšit na 400, 600 a dokonce 1000 ml. Doporučuje se biologický test.
Protein je pasterizovaný 4,3-4,8% roztok plazmatických proteinů, který zahrnuje albumin (75-80%), globuliny (20-25%) s přídavkem železitého albuminu a erytropoetické látky. Protein zaujímá svými vlastnostmi mezipolohu mezi plazmou a albuminem. Infuze proteinového roztoku může být doprovázena alergickými reakcemi, proto by měl být proveden biologický test a měla by být sledována pomalá rychlost infuze.
Krev, na rozdíl od jiných léků s objemovým účinkem, má omezený hemodynamický účinek. Transfúze plné krve a červených krvinek zvyšuje koncentraci krve, což zhoršuje kapilární průtok krve, zejména při šoku a nízkém krevním tlaku. Depozice v kapilárním loži může vytvořit nepřekonatelnou odolnost proti průtoku krve. Mezi faktory, které omezují použití krve jako hlavního média pro ztrátu krve a šok, patří riziko senzibilizace, intoleranční reakce, acidóza způsobená hyperamonémií, zvýšená koncentrace draslíku v krvi, porucha koagulace a možnost virových infekcí.
V naléhavých případech je krevní transfuze prováděna za účelem prevence nebezpečného poklesu globulárního objemu a rozvoje poruch kyslíkové transportní funkce krve s ní spojené. Absolutní indikací pro krevní transfúzi je pokles Ht na 0,25-0,20. Indikací pro transfúzi celé darované krve je akutní masivní ztráta krve v nepřítomnosti složek krve, jako jsou červené krvinky, promyté červené krvinky a čerstvě zmrazená plazma. Ve všech případech akutní posthemoragické anémie v důsledku traumatu, gastrointestinálního krvácení, chirurgického zákroku atd. Je indikována hromadná transfuze erytrocytů. Transfúze promytých červených krvinek je výhodná v případě anemických stavů u pacientů senzibilizovaných opakovanými krevními transfúzemi; u pacientů s anamnézou alergií; s homologním krevním syndromem. Transfúze destiček se provádí s masivní ztrátou krve a masivní náhradou krve, s hemoragickou diatézou způsobenou hlubokou trombocytopenií; ve třetí fázi DIC. Indikací pro transfúzi leukocytů jsou imunosupresivní stavy v purulentních septických procesech, deficit leukocytů při myelotoxické depresi krvetvorby.
ŘEŠENÍ CRYSTALLOID
Tato skupina zahrnuje infuzní roztoky elektrolytů a cukrů. Použití těchto roztoků poskytuje základní (fyziologickou) potřebu vody a elektrolytů a korekci poruch ve vodě, rovnováze elektrolytů a kyselin. Na rozdíl od koloidních roztoků většina krystaloidních roztoků rychle opouští vaskulární lože a přechází do interstitia nebo buněk, v závislosti na jejich složení.
Obvykle lze infuzní roztoky elektrolytů a cukrů (glukózy nebo fruktózy) rozdělit do tří skupin:
1) náhradní roztoky (používané ke kompenzaci ztráty krve, vody a elektrolytů);
2) základní roztoky (zajišťující fyziologickou potřebu vody a elektrolytů);
3) nápravná řešení (používá se k nápravě nevyváženosti iontů, vody a ČOV).
NÁHRADNÍ ŘEŠENÍ
K vyplnění nedostatku izotonického objemu se používají polyelektrolytové roztoky, jejichž osmolarita a složení jsou blízké těmto ukazatelům plazmy a extracelulární tekutiny. Optimální řešení pro tento účel jsou izotonická a isoionická řešení s vyváženým složením. Bohužel jen několik řešení má podobné vlastnosti. Zkušenosti však ukazují, že použití i v nevyvážených situacích (Ringerův roztok, izotonický roztok chloridu sodného) v akutních situacích přináší pozitivní výsledky. Hlavním kritériem pro tyto roztoky by měla být isotonicita nebo mírná hypertonicita, dostatečný obsah složek, které tvoří extracelulární prostředí.
Izotonický (0,85-0,9%) roztok chloridu sodného (fyziologický roztok) byl první roztok používaný k léčbě ztráty krve a dehydratace.
1 litr roztoku obsahuje: Na + - 154 mmol, C1 - 154 mmol. Celková osmolarita je 308 mosm / l, což je o něco vyšší než osmolarita v plazmě. pH 5,5 - 7,0. Koncentrace chloru v roztoku je také vyšší než koncentrace tohoto iontu v plazmě. Proto jej nelze považovat za absolutně fyziologický.
Používá se hlavně jako dárce sodíku a chloru pro ztrátu extracelulární tekutiny. Je také indikován pro hypochloremii s metabolickou alkalózou, oligurii v souvislosti s dehydratací a hyponatrémií. Roztok je dobře kombinován se všemi krevními náhradami a krví. Neměl by být mísen s erytromycinem, oxacilinem a penicilinem. Je nemožné použít jako univerzální řešení, protože v něm je málo volné vody, neexistuje žádný draslík; roztok kyselé reakce, zvyšuje hypokalémii. Kontraindikováno v případě hypernatremie a hyperchlorémie.
Celková dávka je až 2 litry denně. Při intravenózním podání je rychlost infuze 4 až 8 ml / kg tělesné hmotnosti za hodinu.
Ringerův roztok je izotonický roztok elektrolytů, z toho 1 litr obsahuje: Na + - 140 mmol, K + - 4 mmol, Ca + - 6 mmol, C1- 150 mmol. Osmolarita 300 mosm / l. Toto řešení se používá jako náhrada krve od konce minulého století. Ringerovo řešení a jeho modifikace jsou v současné době široce využívány. Jedná se o fyziologický náhradní roztok s mírnými kyselými vlastnostmi.
Používá se k nahrazení ztráty extracelulární tekutiny, včetně krve, a jako nosiče roztoků koncentrátů elektrolytů. Kontraindikováno v případě hyperchlorémie a hypernatremie. Neměl by být smíchán s koncentracemi elektrolytů obsahujících fosfáty.
Dávka - až 3 000 ml / den ve formě kontinuální intravenózní kapací infuze při dávce 120 - 180 kapek / min při 70 kg tělesné hmotnosti.
Infúze soli CIPC je izotonický roztok elektrolytu obsahující různé soli. Vytvořeno během druhé světové války pro léčbu akutní ztráty krve.
1 litr roztoku obsahuje: Na + - 138 mmol, K + -2,7 mmol, Ca + - 2, mmol, Mg2 + - 0,4 mmol, C12 - 144 mmol, S04 "- 0,4 mmol, HCO3 - 1, 6 mmol osmolarity 290 mosm / l.
Infúze soli ZIPK a roztok LIPK-3 doposud neztratily svou hodnotu a lze je použít ke ztrátě izotonických a hypertonických tekutin.
Izotonický a isoionický roztok (ionosteril - "Fresenius") obsahuje ionty ve fyziologicky optimálním poměru (1 l obsahuje: Na + - 137 mmol, K + - 4 mmol, Ca + - 1,65 mmol, Mg + - 1,25 mmol, C1- - 110 mmol, acetát - 36,8 mmol, osmolarita roztoku 291 mosm / l). Používá se jako primární náhradní roztok pro nedostatek plazmatického objemu a extracelulární tekutiny. Kontraindikováno při otoku, hypertenzní dehydrataci, těžkém selhání ledvin.
V závislosti na indikacích se dávka 500-1000 ml nebo více denně podává intravenózně kapací metodou v množství 3 ml / kg / h (70 kapek / min při 70 kg tělesné hmotnosti). V naléhavých případech až 500 ml za 15 minut.
Pro hypotonickou dehydrataci, intravaskulární deficienci objemu se používá isoionický roztok 5% nebo 10% glukózy (fruktózy). Částečně pokrývá potřebu uhlohydrátů. Kontraindikováno při hyperglykémii, hyperhydrataci, hypertonické dehydrataci a metabolické acidóze. Dávka je určena konkrétní situací. Rychlost podávání 3 ml / kg tělesné hmotnosti za hodinu.
Quartasol je izotonický roztok, který se skládá ze čtyř solí (Na + - 124 mmol / L, K + - 20 mmol / L, C1- - 101 mmol / L, HCO3 - 12 mmol / L) a acetátu - 31 mmol / L. Používá se jako náhradní řešení pro polyionické ztráty. Kontraindikováno u hyperkalémie, hypernatremie a hyperchlorémie.
Denní dávka až 1000 ml nebo více, v závislosti na ionogramu. Rychlost podávání 3 ml / kg / h.
Laktasol je fyziologický náhradní roztok s mírnými alkalickými vlastnostmi. Na rozdíl od izotonického roztoku chloridu sodného má Ringerův roztok vyvážené elektrolytové složení blízké složení plazmy.
1 litr roztoku obsahuje: Na + - 139,5 mmol, K + - 4 mmol, Ca2 + - 1,5 mmol, Mg + - 1 mmol, SG - 115 mmol, HCO3 - 3,5 mmol, laktát - 30 mmol. Osmolarita 294,5 mosm / l.
Laktasol a podobný Ringerův roztok laktátu nebo Hartmannův roztok jsou schopny kompenzovat izotonické poruchy v hydroionické rovnováze. Jsou indikovány za účelem nahrazení deficitu extracelulární tekutiny vyváženou acidobazickou rovnováhou nebo mírnou acidózou. Když se přidají do koloidních roztoků a hmoty erytrocytů, zlepšují se reologické vlastnosti výsledných směsí. V důsledku přeměny laktátu sodného na hydrogenuhličitan v těle dochází ke zvýšení kapacity pufru hydrogenuhličitanu a snížení acidózy. Pozitivní vlastnosti laktasolu jako korelátoru poruch vody a elektrolytů jsou však realizovány pouze za podmínek aerobní glykolýzy. Při těžkém nedostatku kyslíku může laktasol zhoršit vznik laktátové acidózy.
Denní dávka laktasolu a Ringerova laktátu je až 2500 ml. Tyto roztoky jsou podávány intravenózně v průměrné rychlosti 2,5 ml / kg / h, tj. asi 60 kapek / min.
Laktasol a Ringerův laktátový roztok jsou kontraindikovány při hypertenzní hyperhydrataci, poškození jater a laktátové acidóze.
ZÁKLADNÍ ŘEŠENÍ
Mezi základní řešení patří roztoky elektrolytů a cukrů, které každodenně potřebují vodu a elektrolyty. Tyto roztoky by měly obsahovat dostatečné množství volné vody, aby se kompenzovala ztráta vody elektrolytem během dýchání a kůží. Současně by tato řešení měla zajistit potřebu základních elektrolytů nebo korigovat mírné abnormality ve složení elektrolytů.
Základní roztok s vysokým obsahem draslíku (Fresenius) obsahuje elektrolyty, dostatečné množství volné vody a uhlohydráty. Jedná se o všestranný alkalický roztok elektrolytu používaný k udržení rovnováhy voda-elektrolyt. Je indikováno, aby vyhovovalo potřebám vody a elektrolytů v těle.
1 l obsahuje: Na + - 49,1 mmol, K + - 24,9 mmol, Mg + - 2,5 mmol, SG - 49,1 mmol, Ä2РО4- - 9,9 mmol, laktát - 20 mmol, sorbitol - 50 g. Obsah kalorií 200 kcal / l. Osmolarita 430 mosm / l.
Tento roztok je kontraindikován při šoku, hyperkalémii, selhání ledvin, otravě vodou, nesnášenlivosti sorbitolu, otravě methanolem.
Roztok se používá ve formě kontinuálního intravenózního kapání. Rychlost podávání 180 ml / h při 70 kg tělesné hmotnosti. Průměrná dávka 1500 ml / m povrchu těla.
Semi-elektrolytový roztok s 5% roztokem glukózy (Fresenius) zajišťuje zavádění vody a elektrolytů s nízkou dávkou uhlohydrátů. Používá se k pokrytí ztrát vody (hypertonická dehydratace); ztráta tekutin chudá na elektrolyty; částečná potřeba uhlohydrátů. Může být použit jako nosič roztoku koncentrátů elektrolytu a léčiv kompatibilních s roztokem.
1 l obsahuje: Na + - 68,5 mmol, K + - 2 mmol, Ca2 + - 0,62 mmol, Mg + - 0,82 mmol, SG - 73,4 mmol, monohydrát glukózy pro injekci - 55 g. Osmolarita 423 mosm / l .
Může být předepsán kontinuální intravenózní infuzí až do 2000 ml / den s průměrnou rychlostí 3 ml / kg tělesné hmotnosti / h.
Kontraindikováno v případě hyperglykémie, přebytečné vody v těle, hypotonické dehydratace.
Infuzní roztok elektrolytu (podle Hartiga) zajišťuje potřebu vody a elektrolytů. Je navržen tak, aby kompenzoval ztráty vody bez elektrolytu a poruchy lehkého elektrolytu. 1 litr obsahuje: Na + - 45 mmol, K- - 25 mmol, Mg + 2 - 2,5 mmol, C1 - 45 mmol, acetát - 20 mmol, Н2РО4- - 10 mmol. Osmolarita 150 mosm / l.
Roztok je kontraindikován při hypotonické dehydrataci a hyperhydrataci, alkalóze, oligurii, šoku.
Rychlost zavádění 3 až 4 ml / kg tělesné hmotnosti / h. Celková dávka je až 1 000 - 2 000 ml / den. Dejte si pozor na předávkování vodou.
5% roztok glukózy je izotonický roztok bez elektrolytů, z toho 1 litr obsahuje 950 ml volné vody a 50 g glukózy. Ten je metabolizován za vzniku H2O a CO2. 1 litr roztoku dává 200 kcal. pH 3,0 - 5,5. Osmolarita je 278 mosm / l. Je indikován k hypertenzní dehydrataci, dehydrataci s nedostatkem volné vody. Základ pro přidání dalších řešení. Kontraindikováno při hypotonické dehydrataci a hyperhydrataci, hyperglykémii, intoleranci, otravě methanolem.
Dávka je určena konkrétní situací. Rychlost podávání je 4 ml / kg / h. Hrozí nebezpečí otravy vodou!
Glukózový roztok 10% - hypertonický roztok bez elektrolytů.
Osmolarita 555 mosm / l. 1 litr roztoku dává 400 kcal. Indikace a kontraindikace jsou stejné jako u 5% roztoku glukózy. Rychlost podávání 2,5 ml / kg / h, v závislosti na indikacích. Hrozí nebezpečí otravy vodou!
Jako a základní řešení lze použít isotonický roztok chloridu sodného, \u200b\u200bRingerův roztok, Ringer-Lockův roztok, laktasol a další izotonické a isoionické roztoky elektrolytů. Všechna tato řešení však nemohou uspokojit každodenní potřeby těla po vodě. Mohou se proto používat společně s elektrolytickými roztoky glukózy nebo fruktózy, přičemž se bere v úvahu základní potřeba vody a elektrolytů.
5% roztok fruktózy, jako roztoky glukózy, je dárcem volné vody a energie (200 kcal / l). Indikace pro použití jsou stejné jako pro roztoky glukózy. Poskytuje náhradu vody bez elektrolytů během horečky, během operace se 10% roztok fruktózy používá zejména v pediatrii. Kontraindikace, dávky a rychlost podávání jsou stejné jako u roztoků glukózy.
NÁPRAVNÁ ŘEŠENÍ
Darrowovo řešení je nápravné řešení používané pro nedostatek draslíku a alkalózu.
1 litr Darrowova roztoku (Fresenius) obsahuje: Na + - 102,7 mmol, K + - 36,2 mmol, C1- 138,9 mmol. Osmolarita je 278 mosm / l.
Indikace pro jeho použití: nedostatek draslíku, alkalóza vyplývající ze ztráty tekutin obsahujících draslík po podání léků na saluretiku a kortikosteroidů.
Naneste až 2000 ml denně ve formě dlouhého kapání intravenózní infuze. Rychlost podávání je asi 60 kapek / min.
Kontraindikováno u hyperkalémie a selhání ledvin.
Roztoky elektrolytu s 5% a 10% roztoky glukózy a vysoký obsah draslíku se používají k nahrazení nedostatku draslíku a ke korekci alkalózy. Tyto roztoky se používají ke ztrátě draslíku a chloridu (například ke ztrátě žaludeční šťávy).
1 litr roztoku elektrolytu s 5% roztokem glukózy obsahuje: Na + - 80 mmol, K + - 40 mmol, C1 - 120 mmol, injekční monohydrát glukózy - 55 g; 50 g glukózy bez krystalizované vody. Obsah kalorií 200 kcal / l, osmolarita 517 mosm / l. Stejný roztok s 10% roztokem glukózy dává 400 kcal / l, jeho osmolarita je 795 mosm / l.
Dávka se stanoví pomocí ionogramových dat. Rychlost podávání 2,5 ml / kg / h. Vzhledem k vysoké koncentraci draslíku nesmí být uvedená rychlost podávání překročena! Maximální dávka: 2000 ml / den s tělesnou hmotností 70 kg.
Tyto roztoky (Fresenius) jsou kontraindikovány v případech acidózy, hyperkalémie, selhání ledvin, přebytečné vody v těle a diabetes mellitus.
Chlosol je izotonický roztok obohacený draslíkem. Přítomnost octanu sodného umožňuje použití chlorsolu k léčbě metabolické acidózy. Tento roztok je indikován pro hypokalémii bez alkalózy, ztráty sodíku a chloru.
1 litr roztoku obsahuje: Na + - 124 mmol, K + - 23 mmol, C1- 105 mmol; acetát - 42 mmol. Osmolarita 294 mosm / l.
Dávka je určena údaji ionogramu. Rychlost vstřikování 4 až 6 ml / kg / h. Roztok je kontraindikován pro hyperkalémii, metabolickou alkalózu, hyperhydrataci a selhání ledvin.
Ionocell (Fresenius) je infuzní roztok pro korekci intracelulární ztráty elektrolytů asparaginátu draselného a hořečnatého.
Přiřazte kombinovaný nedostatek draslíku a hořčíku. Může být použit v předoperačním, intraoperačním a pooperačním období po dobu 2-5 dnů po velkých chirurgických zákrokech. Toto řešení je indikováno pro paralytickou obstrukci ve fázi zotavení po těžkých zraněních a popáleninách. Používá se také po diabetickém kómatu a akutním infarktu myokardu s poruchami srdečního rytmu.
1 litr ionocellového roztoku obsahuje: Na + - 51,33 mmol, K + - 50 mmol, Mg + - 25 mmol, Ca2 + - 0,12 mmol, Zn + - 0,073 mmol, Mn + - 0, mmol, Co - 0,04 mmol, C1- - 51,33 mmol, aspartát - 100,41 mmol. Osmolarita 558 mosm / l.
Dávkování podle údajů ionogramu. Dlouhá intravenózní kapající infuze 1,5 - 2 ml / kg / h nebo maximálně 2100 ml / den s tělesnou hmotností 70 kg. Rychlost podávání je 30-40 kapek / min. Až do maxima 20 mmol draslíku za hodinu.
Ionocell je kontraindikován při těžkém selhání ledvin, hyperkalémii, hypermagnesemii, nesnášenlivosti fruktózy a sorbitolu, otravě methanolem, nedostatku fruktosy-1,6-difosfatázy.
Isotonický roztok chloridu sodného obsahující přebytek chloru, kyselá reakce, se používá pro korekci hypochloremické alkalózy, zejména u oligurie. Je indikováno k vyrovnání ztráty žaludeční šťávy, ale vyžaduje současné zavedení draslíku.
Disol je roztok obsahující dvě soli: chlorid sodný a octan sodný. Je indikován pro korekci hyperkalemického syndromu a hypotonické dehydratace. Roztok může být použit pro ztrátu sodíku a chloru a metabolickou acidózu, v počátečním období oligurie v důsledku dehydratace.
1 litr roztoku obsahuje: Na + - 126 mmol, SG - 103 mmol, acetát - 23 mmol. Osmolarita 252 mosm / l.
Trisol je izotonický roztok obsahující chlorid sodný, chlorid draselný a hydrogenuhličitan sodný. Používá se jako náhrada za Ringerův roztok, zejména s metabolickou acidózou.
1 litr roztoku obsahuje: Na + - 133 mmol, K + - 13 mmol, C1 - 98 mmol, HCO3 - 48 mmol. Osmolarita 292 mosm / l.
Acesol je relativně hypotonický solný roztok obsahující sodík, draslík, chlor a acetát. Používá se k léčbě isotonické dehydratace s mírným posunem rovnováhy voda-elektrolyt. Má alkalizující a protišokový účinek. Pomalé zavedení vám umožňuje použít jej jako základní řešení.
1 litr roztoku obsahuje: Na + - 110 mmol, K + - 13 mmol, C1- 99 mmol, acetát - 24 mmol. Osmolarita 246 mosm / l.
ELEKTROLYTE KONCENTRÁTY (MOLÁRNÍ ŘEŠENÍ)
Molární (5,84%) roztok chloridu sodného se používá k počáteční terapii hluboké hypotonické dehydratace, hyponatrémie, hyperkalémie, hypochloremické alkalózy.
V 1 litru roztoku obsahuje 1 mmol sodíku a 1 mmol chloru. Osmolarita 2000 mosm / l. Podává se podle potřeby, ale ne rychleji než 1 ml / min. Nekompatibilní s erytromycinem, oxacilinem. Kontraindikováno v případě hypernatremie, metabolické acidózy, onemocnění vyžadujících omezení sodíku.
Molární (8,4%) roztok hydrogenuhličitanu sodného je koncentrovaný alkalizační roztok, jehož 1 ml obsahuje 1 mmol hydrogenuhličitanu a 1 mmol sodíku. pH 7,0 - 8,5. Osmolarita 2000 mosm / l.
Používá se při hluboké metabolické acidóze, hypotonické dehydrataci s metabolickou acidózou.
Kontraindikováno u alkalózy, hypernatremie, respirační acidózy, srdečního selhání, plicního edému, eklampsie. Nekompatibilní s dipyridamolem, penicilinem, oxacilinem, vitaminy B, neostigminem.
Dávka 8,4% roztoku (ml) \u003d 0,3 x (-BE) x tělesná hmotnost (kg). Mírná acidóza nevyžaduje korekci. Maximální dávka hydrogenuhličitanu sodného by neměla překročit 1 mmol / kg tělesné hmotnosti. Rychlost vstřikování je 100 ml za 30 minut.
Roztok 7,5% chloridu sodného - hypertonický roztok chloridu sodného (2400 mosm / l). Používá se k léčbě těžké GS bez nebo v kombinaci s dextranem-60, 70. Byla prokázána schopnost fyziologického roztoku pro zvýšení krevního tlaku, srdečního selhání, zlepšení mikrocirkulace a přežití. Objemy transfundované GSH tvoří asi 10% odhadované ztráty krve nebo asi 4 ml / kg tělesné hmotnosti. Zajišťuje výrazný osmotický efekt a pomáhá přitahovat tekutinu do cév interstitia a buněk, což vysvětluje její hemodynamický účinek. 50 ml se injikuje bolus každých 20-30 minut.
Molární (7,49%) roztok chloridu draselného - koncentrovaný roztok. Podává se pouze ve zředěné formě v cukrových roztocích s vhodným množstvím inzulínu. V 1 ml roztoku obsahuje 1 mmol draslíku a 1 mmol chloru. Osmolarita 2000 mosm / l.
Je indikován pro závažný nedostatek draslíku, metabolickou alkalózu a předávkování srdečními glykosidy.
Kontraindikace: anurie a oligurie, hyperkalémie, akutní dehydratace.
Rychlost podávání pro dospělé není vyšší než 20 mmol draslíku za hodinu! Celková dávka není vyšší než 2-3 mmol / kg / den.
Glycerofosfát sodný je koncentrovaný roztok v ampulích. Každý mililitr roztoku obsahuje 1 mmol fosfátu a 2 mmol sodíku. Používá se pro nedostatek fosfátů.
L-asparaginát draselný-hořečnatý je koncentrovaný roztok, jehož 1 ml obsahuje 1 mmol draslíku a 0,25 mmol hořčíku. Je indikován pro hypokalémii a hypomagneziémii, aby se kompenzovaly buněčné elektrolyty.
Používá se pouze jako přísada, používejte ředěný! Maximální dávka je 150 mmol draslíku za den.
Kontraindikováno u hyperkalémie, hypermagnesémie, závažného selhání ledvin.
K prevenci a léčbě nedostatku hořčíku se používá molární (12%) roztok síranu hořečnatého. Profylaktická dávka hořčíku je určena denním požadavkem na tento ion, tj. 5-15 mmol / m. 1 ml tohoto roztoku obsahuje 1 mmol hořčíku a 1 mmol síranu. Osmolarita roztoku je 2000 mosm / l. Aby se zabránilo nedostatku hořčíku, mělo by se denně podávat až 25 ml tohoto roztoku, pokud je hmotnost pacienta 70 kg. K odstranění nedostatku hořčíku se až 30 mmol hořčíku denně podává ve formě přísad do jiných infuzních roztoků. Je přípustné použít 25% roztok síranu hořečnatého, z čehož 1 ml obsahuje 2 mmol hořčíku.
K prevenci a nápravě nedostatku vápníku se používá roztok 10% chloridu vápenatého. Tento roztok se blíží molárnímu roztoku chloridu vápenatého (11%), z čehož 1 ml obsahuje 1 mmol vápníku a 2 mmol chloru. Osmolarita 3 000 mosm / l. 10% nebo 11% roztok chloridu vápenatého je tedy koncentrovaný roztok, který by měl být podáván velmi pomalu, s výhodou jako přísada do jiných infuzních roztoků. Denní potřeba vápníku je 7-20 mmol / m povrchu těla. K nápravě nedostatku vápníku jsou nutné velké dávky (tabulka 25.1).
Tabulka 25.1.
Řešení [od Ya.A. Zhizhevsky, 1994]
| Molární řešení | |||
| Glukóza | 18 | Glukóza 1000 | 1000 |
| Fosforečnan draselný disubstituovaný | 17,41 | Draslík 2000, fosfát 1000 | 3000 |
| Fosforečnan draselný monosubstituovaný | 13,61 | Draslík 1000, fosfát 1000 | 2000 |
| Chlorid draselný | 7,46 | Draslík 1000, chlor 1000 | 2000 |
| Chlorid vápenatý | 11,16 | Calcium 1000, Chlor 2000 | 3000 |
| Síran hořečnatý | 12 | Hořčík 1000, síran 1000 | 2000 |
| Chlorid hořečnatý | 9,53 | Hořčík 1000, Chlor 2000 | 3000 |
| Hydrogenuhličitan sodný | 8,4 | Sodík 1000, hydrogenuhličitan 1000 | 2000 |
| Laktát sodný | 11,4 | Sodík 1000, laktát 1000 | 2000 |
| Fosforečnan sodný disubstituovaný | 12,2 | Sodium 2000, Fosfát 1000 | 3000 |
| Fosforečnan sodný monosubstituovaný | 12 | Sodík 1000, fosfát 1000 | 2000 |
| Chlorid sodný | 5,85 | Sodík 1000, chlor 1000 | 2000 |
| Kyselina chlorovodíková | 3,65 | Vodík 1000, chlor 1000 | 2000 |
| Izotonická řešení | |||
| Glukóza | 5,5 | Glukóza 3000 | 300,5 |
| Chlorid kademnatý | 1,46 | Draslík 148, chlor 148 | 296 |
| Chlorid vápenatý | 1,1 | Calcium 99, Chlor 198 | 297 |
| Síran hořečnatý | 11,75 | Hořčík 146, síran 146 | 292 |
| Chlorid hořečnatý | 0,95 | Hořčík 99,5, chlor 199 | 298,5 |
| Hydrogenuhličitan sodný | 1,25 | Sodík 149, hydrogenuhličitan 149 | 298 |
| Laktát sodný | 1,65 | Sodík 145, laktát 145 | 290 |
| Chlorid sodný | 0,85 | Sodík 145, chlor 145 | 290 |
| Hypertonická řešení | |||
| Glukóza | 10 | Glukóza 555 | 555 |
| » | 20 | Glukóza 1110 | 1110 |
| Chlorid vápenatý | 10 | Calcium 901, Chlor 1802 | 2703 |
| Chlorid sodný | 10 | Sodík 1710, chlor 1710 | 3420 |
| Síran hořečnatý | 25 | Hořčík 2083, síran 2083 | 4166 |
Roztoky mannitolu (10% a 20%) jsou hyperosmolární roztoky diurézy stimulující hexatomický alkohol s obsahem mannitolu. Osmolarita 20% roztoku mannitolu je 1372 mosm / l. Tělo není metabolizováno a vylučováno ledvinami. Hlavní indikací je prevence a léčba funkčního selhání ledvin, mozkový edém. Protože mannitol způsobuje přechodnou hypervolémii, neměl by být používán při akutním srdečním selhání a při vysoké CVP. Kontraindikováno při dekompenzovaném selhání ledvin.
Jedna dávka 20% roztoku je 250 ml. Zadejte po dobu 30 minut rychlostí 250 ml Denní dávka je 1-1,5 g / kg tělesné hmotnosti, ale ne více než 100 g.
Roztok sorbitolu (40%) se používá pro stejný účel jako roztoky mannitolu. Jedna dávka - 250 ml. Rychlost podávání 250 ml za 30 minut Přes den, podle indikací, stejná dávka každých 6-12 hodin.
DETOXIKAČNÍ ŘEŠENÍ
Tato infuzní média jsou koloidy vinylových sloučenin s nízkou molekulovou hmotností. Jejich frakce s nízkou molekulovou hmotností má vlastnosti, které je přibližují proteinům. Tyto roztoky vážou cirkulující toxiny, zlepšují reologické vlastnosti krve a mají diuretický účinek, který pomáhá vylučovat toxiny z krevního řečiště. Protože většina toxických metabolitů má krtek. hmotnost asi 500-5000, jejich vazba je možná u látek s přibližně stejným molem. hmotnost. Vazba toxinů je zajištěna vysokou adsorpční kapacitou těchto syntetických polymerů.
Tato skupina zahrnuje hemodézu, hemodes-H, neohemodézu vytvořenou na bázi polyvinylpyrrolidonu a polydez na bázi polyvinylalkoholu. Detoxikační účinek těchto léčiv je zvýšen díky jejich vysoké koloidní osmotické aktivitě, která vede ke zvýšenému hemodiluci a produkci moči s rychlou eliminací toxinů spolu s polymerem.
Hemodez - 6% roztok polyvinylpyrrolidonu-N s nízkou molekulovou hmotností, má vysokou komplexační aktivitu, má mol. hmotnost 12 000 ± 2700. Složení hemedů, kromě polyvinylpyrrolidonu, zahrnuje chlorid sodný, draslík, vápník a hořčík, hydrogenuhličitan sodný. Zlepšení reologických vlastností krve je spojeno s nízkou viskozitou (relativní viskozita 1,5-2,1), účinkem redepozice albuminu a ředěním krve. Tento efekt se projeví pouze v případě, že nedochází k zásadním změnám hemodynamiky a šoku.
Indikace pro použití hemodézy jsou intoxikace různého původu, hnisavé septické procesy, těžké popáleniny, katabolická fáze pooperační periody, exogenní otrava. Hemodéza je kontraindikována u kardiopulmonální dekompenzace, hemoragické mrtvice, bronchiálního astmatu a akutní nefritidy.
Hemodezní roztok se používá pomalou intravenózní infuzí rychlostí 40-50 kapek / min v dávce ne vyšší než 5 ml / kg tělesné hmotnosti denně (s výhodou ve 2 dávkách). Se zvýšením rychlosti podávání, kožní hyperémie, snížením krevního tlaku, pocitu nedostatku vzduchu. V těchto případech by infuze hemodézy měla být okamžitě zastavena.
Cizí analogy hemodézy: periston-N, nekompenzované.
Polydez je 3% roztok alkoholu s nízkou molekulovou hmotností. Průměrný mol. hmotnost 10 000 ± 2000. Má výrazný detoxikační účinek, netoxický, bez pyrogenů, neantigen. Nízké molo. Hmota přispívá ke stimulaci diurézy a její rychlé filtraci v ledvinách. Reologický účinek je způsoben rozložením krevních buněk.
Složení roztoku polydezu: polyvinylalkohol-N - 30 g; Na + - 154 mmol / 1; C1- - 154 mmol / L. Osmolarita 308 mosm / l.
Indikace pro jmenování polydez a kontraindikace jsou stejné jako u hemodezu.
Polydez se podává intravenózně pouze metodou kapání při rychlosti ne více než 20-40 kapek / min. Celková dávka pro dospělé není větší než 400 ml / den ve dvou rozdělených dávkách. Při zrychleném podávání jsou možné závratě a nevolnost.
Při těžkých zraněních, syndromu dlouhodobého komprese, patologických procesech, které se vyskytují při těžké endotoxémii, včasné užívání těchto léků zabraňuje rozvoji akutního selhání ledvin.
INFUZNÍ ŘEŠENÍ POLYFUNKČNÍ AKCE
Některá nová infuzní média mají zřetelný multifunkční účinek: hemodynamický, reologický, detoxikační, diuretický atd. Mezi multifunkční léky se nejčastěji používá polyvisolin, polyoxidin, reogluman a mafusol.
Polyvisolin, vytvořený na bázi polyvinylalkoholu s molem. o hmotnosti 10 000, má zřetelný účinek proti nárazům a detoxikaci.
Polyoxidin, vytvořený na bázi polyethylenglykolu s mol. o hmotnosti 20 000, se používá při léčbě šoku. Tento lék má výrazný reologický a detoxikační účinek.
Reogluman - 10% roztok dextranu s molem. o hmotnosti 40 000 v 0,9% roztoku chloridu sodného a 5% roztoku mannitolu. Má výrazný reologický účinek (snížení intravaskulární agregace, zlepšená mikrocirkulace) a detoxikační účinek. Používá se při těžkých zraněních, popáleninách, při cévní chirurgii, po období po resuscitaci.
Vstupte intravenózně rychlostí až 40-60 kapek / min s povinným provedením biologického testu. V prvních 10 - 15 minutách by rychlost infuze neměla překročit 5 - 10 cap / min, doporučuje se přestávky, aby se stanovila možná reakce na léčivo. Denní dávka pro dospělé je až 400-800 ml.
Methusol je solný infuzní roztok s antihypoxantem - fumarátem sodným. Fumarát je v těle metabolizován produkcí ATP, což je zvláště důležité při léčbě těžkých pacientů s anaerobní glykolýzou. Klinické studie ukázaly, že methusol je účinné antihypoxické léčivo a je druhem regulátoru tkáňového metabolismu. Současně má tento lék také anti-shock efekt.
KRVNÉ NÁHRADY S FUNKCÍ PŘEPRAVY PLYNU
Tato skupina zahrnuje léčiva, která mohou vykonávat funkci transportu kyslíku a CO2 bez účasti hemoglobinu a červených krvinek.
Akutní masivní ztráta krve nevyhnutelně vede ke změnám v systému přenosu kyslíku v hypoxii krve a tkání. Pokud je problém léčby akutní hypovolémie a souvisejícího oběhového selhání v současné době docela úspěšně vyřešen vytvořením významného arzenálu hemodynamických a protišokových infuzních médií, problém adekvátního nahrazení deficitu objemu cirkulujících červených krvinek je stále daleko od konečného řešení. Jeho řešení závisí na tvorbě nových léků - nosičů krevních plynů bez účasti krevních buněk, tj. skutečné krevní náhražky.
V mnoha zemích: v Japonsku, USA, Francii, Anglii a Rusku se provádí vyhledávání a připravují se přípravky na bázi plně fluorovaných uhlovodíkových sloučenin - perfluorovaných uhlovodíků. Jedná se o chemicky neaktivní látky, jejichž všechny atomy vodíku jsou nahrazeny atomy fluoru. Možnost použití perfluorovaných uhlovodíků byla studována od roku 1966. V experimentu bylo prokázáno, že myš, úplně ponořená do emulze perfluorouhlíků, v ní žila mnoho hodin. Výměna krve u myší emulzí perfluorouhlovodíků také ukázala své pozitivní vlastnosti. V roce 1979 byly perfluoruhlovodíky poprvé použity k infuzi u lidí.
V roce 1973 byl v Japonsku vytvořen Fluosol-DA-20, což je emulze plně fluorovaných sloučenin, včetně perfluorodecainu, perfluortripropylaminu, glycerinu, hydroxyethylového škrobu, sodíku, draslíku, chloridů hořčíku a hydrogenuhličitanu sodného.
V roce 1985 byly v naší zemi vytvořeny přípravky „perfluoran“ a „perfucol“ v blízkosti fluosolu.
Perfluorované uhlovodíky mají výrazné transportní vlastnosti kyslíku. Mohou dodávat kyslík do oblastí, kde je obtížné zásobovat krev. Vysoká propustnost perfluorovaných uhlovodíků je způsobena skutečností, že velikost částic emulze je menší než velikost červených krvinek. Proto našli uplatnění při léčbě infarktu myokardu a dalších stavů způsobených zvýšenou trombózou.
Všechny přípravky patřící do skupiny perfluorovaných uhlovodíků první generace mají společné nevýhody: nízká kapacita kyslíku, nízká stabilita, dlouhá retence v těle a krátká doba oběhu ve vaskulárním loži. Klinické studie odhalily reaktogenitu. V současné době probíhá výzkum vývoje nové generace perforovaných organických sloučenin povrchově aktivních látek. Při záchraně obětí hromadných katastrof je obtížné přeceňovat potřebu vytvořit skutečné krevní náhražky, které poskytují funkci přenosu kyslíku.
Vlastnosti hlavních představitelů skupin infuzní roztoky, jejich dávky, indikace k použití a možné komplikace jsou uvedeny v souhrnné tabulce. 25.2.
NOVÉ PLASMOVÉ NÁHRADY
Chaes-steril (HAES-steri1, "Frezhenius Kabi") je roztok hydroxyethyl polysacharidu s průměrným molem. hmotnost 200 000 a 50% substituce vazeb v molekule; umělý koloidní komplex sestávající z rozvětvených řetězců amylopektinu.
Farmakologické vlastnosti: má účinek nahrazující objem a má pozitivní vliv na systémovou hemodynamiku, kapilární průtok krve a reologické vlastnosti krve, zvyšuje osmotický tlak plazmy, pomáhá eliminovat metabolické poruchy. V krvi se štěpí na molekulární velikost 70 000, stimuluje diurézu a ledvinami je snadno vylučuje.
Použití HAEC-sterilu je indikováno ve všech případech akutní ztráty krve, s hemoragickým, traumatickým a popáleninovým šokem, akutní hypovolémií a chirurgickými zásahy k doplnění a udržení objemu krve.
6% a 10% HAEC-sterilní roztoky jsou k dispozici v 250 ml a 500 ml lahvích.
Roztok HAEC-sterilního 6% má průměrný mol. hmotnost 240 000. Průměrná doba trvání jeho působení je 3–4 hodiny se 100% mírným efektem plató.
Roztok HAEC-sterilního 10% má průměrný mol. hmotnost 200 000. Průměrná doba trvání jeho působení je více než 3 až 4 hodiny s počátečním plató efektem 145%.
Roztoky HAEC-sterilního rychle obnovují snížený BCC, normalizují kapilární průtok krve, poskytují dostatečně dlouhý intravaskulární účinek, snižují hematokrit a viskozitu krve a vylučují hyperkoagulační vlastnosti plazmy. Riziko alergických reakcí je extrémně nízké. Tabulka 25.2.
Infuzní roztoky
Nejúplnější principy infuzní terapie formuloval Dennis (1962). Zahrnují:
Přiměřené zajištění fyziologických potřeb těla v iontech a vodě;
Náprava nedostatku iontů a vody;
Kompenzace současných patologických ztrát iontů a vody.
Každý lékař, který zahájí léčbu pacienta se zhoršeným metabolismem voda-sůl mentálně (nebo lépe písemně), určí algoritmus, který může být reprezentován v následující sekvenci:
1. Určete míru porušení rovnováhy voda-sůl a kyselá báze, stanovte stupeň nedostatku nebo nadbytku iontů a vody, rychlost výskytu porušení;
2. Pomocí údajů z anamnézy, předběžných laboratorních testů, výsledků vyšetření pacienta, stanovení formy porušení rovnováhy voda-sůl a acidobazická rovnováha;
3. Určete čas, během kterého je oprava porušení plánována. V nekomplikovaných případech se obvykle provádí korekce během jednoho dne, u těžkých pacientů však může být tato doba zkrácena na 3-4 hodiny. Zároveň se u novorozenců může tato fáze zvýšit až na 3–8 dní;
4. Vypočítejte rychlost podávání léčiva, pečlivě sledujte stav hemodynamiky (CVP, srdeční frekvence, krevní tlak atd.) A renální funkce. U dospělých je maximální rychlost podávání 500 ml / hod., Avšak při šokových podmínkách může být významně zvýšena;
5. V závislosti na formě narušení metabolismu voda-sůl a kyselá báze je nezbytné stanovit složení a pořadí zavedení nápravných roztoků;
6. Ověřit účinnost terapie pomocí klinických a laboratorních testů;
7. Po dříve stanoveném „kontrolním“ čase (čím těžší je pacient, tím vhodnější je „kontrolní“ čas, který zabere méně: 3, 6, 12 hodin), přehodnocuje závažnost pacienta, formy porušení, způsoby korekce, složení a rychlost podání. Infúzní média a znovu sestavit program pro další léčbu pacienta.
Prezentovaná posloupnost účinků umožňuje postupné vyřazování a pod stálou kontrolou k odstranění pacienta ze závažného stavu.
Zároveň je pro postupné stažení nutné, aby každý lékař určil rozsah úkolů, které budou řešeny pomocí infuzní terapie. V podstatě jde o následující:
Odstranění deficitu bcc, udržení adekvátní krevního oběhu, zejména při pokračující patologické ztrátě vody, červených krvinek, iontů;
Kompenzace za tzv. Současné patologické ztráty, které mohou být způsobeny častým zvracením, přítomností drenáže ve střevech, ztrátou tekutiny z povrchu těla a plic při zvýšené teplotě a tachypnoe (pocení);
Zajištění těla pacienta během dne nezbytnou normou vody a iontů;
Stanovení složení, rychlosti a délky zavádění nápravných řešení;
S dlouhou, na několik dní, korekcí porušení metabolismu voda-sůl a CBS, zkuste poskytnout paralelně parenterální výživa pacient.
Úkoly nejsou ničím jiným než programem infuzní terapie pacienta.
K vyřešení těchto problémů nejčastěji používají zavádění tekutin do centrálních žil, do kterých je dříve zaveden katétr.
Katetrizace centrálních (subklaviálních, jugulárních, femorálních) žil nepochybně přináší řadu výhod: spolehlivost, schopnost značně měnit rychlost podávání, injikovat roztoky se složkami, které dráždí intimu cévy; možnost odběru krve pro analýzu; udržení aktivity pacienta během infuze a prodloužený přístup do žíly. Je však třeba poznamenat, že dlouhodobý pobyt katétru ve vaskulárním lůžku ukládá personálu další povinnosti, pokud jde o prevenci purulentních septických komplikací spojených s katetrizací centrálních žil. Proto punkce periferních žil neztratila svůj význam.
Venezekce neztratila svůj význam, hlavní výhodou je vizuální kontrola zavedení a spolehlivosti katétru. V těchto případech se však zánětlivé procesy ve vnitřních cévách rychle rozvíjejí a mohou být udržovány průchodné po dobu maximálně 3 až 4 dnů. Obvykle se za tímto účelem uchylují k počátečnímu úseku v. safena magna v oblasti středního kotníku.
Nevýhody spojené s venezekcí jsou během katetrizace periferních žil výrazně sníženy. V současné době mnoho západních firem vyrábí sady jehel, vodítek a katétrů pro proražení a katetrizaci periferních žil. Nejčastěji je tímto způsobem katetrizována krychální žíla. Při správné péči může katétr fungovat po dobu 4 až 6 dnů, po kterých se objeví flebitida. Další výhodou tohoto způsobu je to, že katetrizovaná nádoba není ovázaná.
Podobným způsobem mohou být cévy katetrizovány poté, co byly chirurgicky izolovány od okolních tkání. Výhodou této metody je to, že katetrizace se provádí za vizuální kontroly.
Jak jsme však již naznačili, od 60. let se dává přednost katetrizaci centrálních žil podle Seldingera. Nejčastěji se k tomu používá: v. subklavie, v. jugularis interna et externa, v. femoralis. Je však třeba si uvědomit, že technika provedení propíchnutí cévy s sebou nese řadu závažných komplikací: propíchnutí tepen, poškození plic (s propíchnutím subklaviální žíly), jícnu, průdušnice a dokonce i srdce.
V souvislosti se závažnými komplikacemi, které se vyskytují jak při venepunkci, její katetrizaci, tak i při dlouhém katétru je nutné striktně dodržovat techniku \u200b\u200bvpichu a pravidla péče o katétr.
Indikace propíchnutí centrálních žil jsou:
1) potřeba masivní infuzní terapie (šok) a možnost chirurgického zákroku u tohoto pacienta;
2) potřeba dlouhodobé infuzní terapie a parenterální výživy;
3) potřeba častého odběru krve za účelem kontroly probíhající terapie;
4) potřeba zavádění léků, které způsobují podráždění cévní intimy;
5) nemožnost propíchnutí periferních žil.
Manipulace by měla být prováděna na operačním sále, místo vpichu by mělo být dobře anestetizováno, ruce lékaře a místo vpichu jsou považovány za operaci.
V případě selhání by nemělo být provedeno několik vpíchnutí kůže - jedná se o další vstupní bránu pro infekci. Směr jehly můžete změnit z jedné injekce. Pokud jste nebyli schopni propíchnout žílu po dobu 10-15 minut, nepředpokládejte, že vás to diskredituje jako lékaře. Nejrozumnější věc v této situaci je uklidnit se a nabídnout punkci jinému lékaři (i začátečníkům). Neužívejte bolestivě selhání, k tomu dochází iu zkušených lékařů, je lepší to zkusit analyzovat. To obohatí vaše zkušenosti.
K určení optimální polohy katétru v žíle je nutné znát lineární rozměry použitých nástrojů: jehly, katétry, vodiče.
Směr jehly by se měl měnit pouze při vyjímání pod kůži, protože „hledání žíly“ může být doprovázeno jeho prasknutím.
Nepoužívejte vodiče (rybářská šňůra) zkroucené pod malými průměry, protože to může přispět k nodulaci a řezání vodiče.
Po katetrizaci cévy je nutné v ní stanovit hloubku katétru. Optimální poloha je poloha katétru, když hladina tekutiny v něm s každým dechem pacienta vstoupí z vnějšího konce. V tomto případě je distální (cévní) konec katétru umístěn ve střední nebo dolní části nadřazené vévy.
Kůže v místě katétru by měla být často ošetřována antiseptiky (1% roztok brilantní zelené, "Lifusol").
Dodržování těchto norem by mělo být pravidlem pro zdravotnický personál provádějící katetrizaci žil a zajišťující péči o katétr.
Považujeme za vhodné popsat techniku \u200b\u200bkatetrizace subclaviánské žíly.
Se subklaviánským přístupem lze použít několik bodů v subklaviánské oblasti: body Aubaniak, Wilson a Giles. Aubaniakův bod je umístěn 1 cm pod klíční kostí podél linie dělící vnitřní a střední třetinu klíční kosti; Wilsonův bod 1 cm pod klíční kost ve střední klíční linii; Giles směřuje - 1 cm pod klíční kost a 2 cm směrem ven od hrudní kosti. U dospělých je bod Aubaniak nejčastěji používán k defektu. Jehla jde k hornímu okraji sternoclavikulárního kloubu, takže injekce mezi jehlou a klíční kostí je 45 ° a do roviny hrudníku - 25 °. Trvalým tahem pístu stříkačky naplněné novokainem nebo solným roztokem pomalu vpřed jehlu ve zvoleném směru (aniž by se měnila!). Vzhled krve v injekční stříkačce naznačuje pronikání špičky jehly do lumenu cévy. Pokud se krev neobjeví v injekční stříkačce, ale jehla vstoupila do tkáně dostatečně hluboko, je nutné ji pomalu začít odebírat v opačném směru (směrem k sobě), přičemž ve stříkačce bude nadále vytvářet vakuum. Stává se, že jehla prochází oběma stěnami a krev vstupuje do lumenu jehly, pouze pokud je odstraněna v opačném směru. Poté se injekční stříkačka odpojí a přes lumen jehly se zavede vodič. Pokud vodič neprochází, je vhodné otočit jehlou kolem její osy. Podle našeho názoru je změna polohy jehly v žíle, jak doporučuje V. D. Malyshev (1985), nepřijatelná, protože s sebou nese nebezpečí prasknutí žíly. Nesmí být dovoleno nucené propagace dirigenta a jeho zpětné extrakce. Ten je spojen s nebezpečím řezání vodiče a jeho zavedení do nádoby. Po vyjmutí jehly z vodiče se polyethylenový katétr vloží do požadované hloubky čistými rotačními pohyby. Připojením stříkačky ke katétru určují správnou polohu: do stříkačky by měla volně proudit krev. Katétr je naplněn roztokem heparinu - 1 000 jednotek na 5 ml isotonického roztoku NaCl. Kanyla katétru je uzavřena zátkou, která je pokryta sterilní vložkou. Někteří lékaři fixují katétr na kůži pomocí stehu. Místo vpichu musí být ošetřeno brilantně zelenou barvou a je lepší ji zakrýt aerosolem Lifuzol, který je na kůži fixován baktericidní adhezivní náplastí.
Se supraclavikulárním přístupem je injekční bod umístěn v rohu tvořeném laterální nohou sternocleidomastoidního svalu a klíční kosti. Jehla směřuje ke spodnímu okraji sternoclavikulárního kloubu, jeho sklon vzhledem k pokožce je 15 °. Další manipulace se provádějí ve stejném pořadí jako se subklaviánským přístupem.
Vnitřní jugulární žíla je propíchnuta pouze zprava, protože propíchnutí levé jugulární žíly představuje riziko poškození hrudního lymfatického kanálu. Pacient je položen stejně jako pro vpich subclaviánské žíly. Jehla se vstříkne mezi nohy stehenního svalu 1 - 1,5 cm nad sternoclavikulárním kloubem. Jehla by měla svírat úhel se sagitální rovinou 60 ° as povrchem kůže - 30 - 45 °.
Katetrizace vnější krční žíly se provádí po chirurgické izolaci.
Pro provádění infuzních terapií se používají systémy pro jedno použití, u nichž je velikost trysek navržena tak, že objem kapky je 0,05 ml. Proto 1 kapka bude obsahovat 20 kapek. Pro stanovení rychlosti zavádění roztoků v cap / min je nutné rozdělit objem plánované infuze na ranní dobu, během níž se má infuze provádět: n \u003d V: 3 t.
Kde n je počet kapek za minutu;
V je objem infuze v ml;
3t je trojnásobná doba, po kterou je roztok podáván.
Pokud se předpokládá, že infuze bude provedena během dne, můžete použít následující vzorec: n \u003d V F,
Kde n je počet kapek za minutu;
V je objem tekutiny nalité během dne v litrech;
F je faktor 14.
Práce v oddělení by měla být nastavena tak, aby systém transfúze kapalin fungoval déle než jeden den.
Fyziologické potřeby vody a bazických iontů.
Potřeba vody zdravého nebo nemocného těla je dána celkovou hodnotou jeho vylučování z těla močí, kůží, povrchem plic, stolicí. U dospělých je potřeba vody 40 ml / kg denně (V. A. Negovsky, A. M. Gurvich, E. S. Zolotokrylina, 1987), denní potřeba sodíku je 1,5 mmol / kg, v vápníku - přibližně 9 mmol (10 ml 10% roztoku glukonátu nebo chloridu vápenatého) a denní potřeba hořčíku je 0,33 mmol / kg. Množství 25% síranu hořečnatého lze stanovit podle vzorce:
Celkový denní požadavek (MgS0) v mmol: 2 \u003d ml / den.
Je žádoucí zavést chlorid draselný do roztoku glukózy s inzulínem, ale jeho koncentrace by neměla překročit 0,75% a rychlost podávání je 0,5 mmolDkg za hodinu). Celková dávka draslíku by neměla překročit 2-3 mmolDkg kg).
Fyziologická potřeba tekutin je kompenzována solnými roztoky a 5-10% roztokem glukózy v poměru 1: 2 nebo 1: 1.
Dalším krokem při provádění infuzního programu je kompenzovat nedostatek tekutin a iontů a současné patologické ztráty v těle pacienta. Je třeba poznamenat, že tento problém by měl být vyřešen v první řadě, protože právě zde je úspěch léčby položen v mnoha ohledech.
Rozlišujte mezi fyziologickými a patologickými ztrátami. Vyhlídka u dospělých je tedy 0,5 ml / kg za hodinu. Ztráty při diuréze jsou normální 1 ml / kg za hodinu.
Znalost fyziologických ztrát je zvláště důležitá a nezbytná při provádění infuzní terapie u pacientů se selháním ledvin, protože údaje uvedené pro denní potřeby tekutin již zahrnují fyziologické ztráty. Neméně důležité je zohlednění patologických ztrát, které mohou dosáhnout významných hodnot. S hypertermií (více než 37 °) a zvýšením tělesné teploty o 1 ° se tedy ztráta vody v průměru zvyšuje o 500 ml denně. Voda uvolněná potem obsahuje 20-25 mosmol / l Na a 15-35 mosmol / l SG. Ztráty se mohou zvyšovat s horečkou, tyrotoxickými krizemi, s některými z nich léky (pilokarpin), vysoká okolní teplota.
Ztráta vody stolicí u dospělých je normální asi 200 ml / den. Trávení je doprovázeno uvolňováním asi 8 až 10 litrů vody s ionty rozpuštěnými v lumen žaludku a střev. Ve zdravém střevě je téměř celý tento objem reabsorbován.
Při patologických stavech (průjem, zvracení, píštěle, obstrukce střeva) tělo ztrácí značné množství vody a iontů. V případě narušení absorpčních procesů ze střeva se vytvoří transcelulární bazény, které oddělí velké množství vody a elektrolyty. Pro přibližnou korekci se doporučuje, aby se při vývoji střevní parézy II. Stupně zvýšil objem tekutiny o 20 ml / (kg den), III stupeň - o 40 ml / (kg den). Nápravné roztoky by měly obsahovat sodík, draslík, chlor atd.
Časté zvracení způsobuje nedostatek vody v průměru 20 mlDkg denně) a korekce se nejlépe provádí pomocí roztoků obsahujících chloridy a draslík.
Při mírném průjmu se doporučuje náhrada tekutin v dávce 30-40 ml / (kg den), se silným průjmem - 60-70 ml / (kg den) a se silnou - až 120-40 ml / (kg den) u roztoků obsahujících ionty sodík, draslík, chlor, hořčík.
V případě hyperventilace je vhodné podat 15 ml / (kg den) roztoku glukózy pro každých 20 respiračních pohybů nad normální hodnotu. Při provádění mechanické ventilace bez dostatečné hydratace dochází ke ztrátě až 50 ml / h, tj. Ventilace zařízením typu RO-6 během dne vyžaduje další vstřikování 1,5 až 2 litrů kapaliny.
Nejideálnějším a nejkompetentnějším způsobem, jak opravit patologické ztráty, je určit složení ztraceného média a jejich množství. V tomto případě je možné přesně napravit stávající porušení i při použití oficiálních řešení.
Tabulka 21.
Používá se v infuzní terapii (podle Yu. N. Shanin et al., 1976).
Při výpočtu a výběru různých infuzních médií existují určité obtíže při převodu množství látky obsažené v roztoku na mmol a naopak. Proto níže uvádíme takové poměry pro nejpoužívanější látky.
Takže v 1 ml obsahuje:
7,4% roztok KG-1 mmol K * a 1 mmol O "3,7% roztoku KCl-0,5 mmol K a 0,5 mmol Cl ~ 5,8% roztok NaCl-1 mmol Na a 1 mmol Cl ~ 8, 4% roztok NaHCO - 1 mmol Na a 1 mmol HCOf
4,2% roztok NaHCO - 0,5 mmol Na a 0,5 mmol HCO ~ \u200b\u200b10% roztok CaCl - 0,9 mmol Ca + a 1,8 mmol Cl ~ 10% roztok NaCl - 1,7 mmol Na a 1,7 mmol Ct 25% roztok MgS0 - 2,1 mmol Mg a 2,1 mmol SO / "1 mol se rovná:
| Na + | 23 g | NaCl | 58,5 g |
| C + - | 35,5 g | KC1 | 74,5 g |
| Do | 39 g | NaHCC | - 84 g |
| Sa ++++ | 40 g | Cacl | 111 g |
| Mg ++ | 24 g | ||
| Hcof | 61 g |
Objem koloidů závisí nejprve na závažnosti hemodynamických poruch a stavu volémie; za druhé, z potřeby zavedení krevních náhrad ze zdravotních důvodů (například v případě krvácení - zavedení plazmy, krve).
Výběr tak zvaného „výchozího roztoku“ bude také záviset na stupni dehydratace a jeho formě. Vysvětlíme tento nápad. Třetí stupeň dehydratace nastává se silnými hemodynamickými poruchami a měl by být považován za hypovolemický šok. V tomto ohledu by navzdory formě dehydratace mělo být zahájeno ošetření léky, které vyvolávají volemický účinek (albumin, reopoliglyukin, hemodéza), po kterém je nutné pokračovat s zaváděním tekutin v závislosti na formě dehydratace. Je tedy vhodné zahájit léčbu extracelulární dehydratace (exicosis s nedostatkem soli) zavedením izotonického roztoku chloridu sodného. Zavedení 5% glukózy je kontraindikováno, protože její rychlý pohyb do intracelulárního sektoru může způsobit mozkový edém. Na rozdíl od dehydratace buněk se jako výchozí roztok doporučuje 5% roztok glukózy. Způsobuje určitou hypotonicitu extracelulárního sektoru a zajišťuje nasycení intracelulárního prostoru vodou. U syndromu celkové (obecné) dehydratace se doporučuje zahájit terapii izotonickým roztokem glukózy, načež následuje přechod na podávání isotonických solných roztoků.
Při provádění infuzní terapie během císařského řezu nebo při porodu je třeba mít na paměti, že zavedení roztoků glukózy před porodem je indikováno pouze u žen se zpočátku nízkou hladinou cukru. To je způsobeno skutečností, že příjem glukózy do plodu prostřednictvím uteroplacentálního krevního řečiště způsobuje hyperinzulinémii, která po odstranění plodu a zastavení glukózy od matky může způsobit hypoglykémii a zhoršit stav novorozence. Po odstranění dítěte se obvykle podává glukóza a fyziologický roztok v poměru 1: 1.
Celkový objem tekutiny potřebné k nápravě nedostatku a denní potřeba závisí na stupni dehydratace. Důležitým kritériem pro jeho stanovení jsou klinická a laboratorní data.
Dalším úkolem, který je třeba vyřešit, je určit čas, během kterého je plánováno provedení korekce dehydratace. Je vhodné dodržovat zásadu, že celkový objem vstřikované tekutiny (enterální a intravenózní) by měl být v rozmezí 5 - 9% tělesné hmotnosti a přírůstek hmotnosti by neměl překročit tato čísla, protože ukazují limit kompenzačních schopností kardiovaskulárního a močového systému. Podle V. M. Sidelnikov (1983) by měl být deficit vody a solí kompenzován za 24-36 hodin a 60% deficitu vody by mělo být zavedeno během prvních 12 hodin. U pacientů se srdečním selháním může být tato doba prodloužena na 3 až 5 dní. Finberg (1980) doporučuje, aby polovina denního požadavku byla zavedena za 6-8 hodin, a zbytek, plus částka patologické ztráty, by měly být hodiny zbývající do konce dne.
Kritéria pro adekvátní infuzní terapii jsou:
I. Hemodynamické ukazatele:
Stav toku periferní krve (mikrocirkulace), plnění safénových žil; ortostatický test (když pacient vstane, vyhodnotí se dynamika pulsu - jeho zvýšení, vyjádřené v%, odpovídá procentu deficitu salvy) krevní tlak, puls, CVP.
Při provádění infuzní terapie, zejména masivní, je nutné se zaměřit na ukazatele CVP. Je třeba připomenout, že normální hodnoty pro dospělé jsou 50–120 mm vody. Art.
CVP odráží v první řadě objem nízkotlakého systému, plnění pravých částí srdce krví. CVP do určité míry nepřímo charakterizuje BCC, pokud pacient nemá žádné srdeční selhání. Nebyl identifikován žádný přímý vztah mezi BCC a CVP.
Zvýšení CVP lze pozorovat se zvýšením (nebo zablokováním) tlaku v plicní tepně, mechanickou ventilací, zejména s pozitivním tlakem na konci výdechu, a zvýšením dolních končetin. Snížení indexů CVP může znamenat narušení průtoku krve do pravého srdce, například když je spodní dutá vena cava osvícena těhotnou děloží, přetížení spodní vena cava po vložení válce pod záda pacienta nebo použití extradurálního nebo gangliového bloku.
Pokud neexistují žádné viditelné důvody pro zvýšení CVP, pak je to pravděpodobně způsobeno dvěma faktory: slabostí srdce nebo zvýšením BCC. Je třeba poznamenat, že při srdečním selhání, ke kterému dochází na pozadí hypovolémie, mohou být parametry CVP normální. Žilní hypertenze je indikována, když CVP překročí 150 mm vody. Art.
Žilní hypotenze (CVP pod 30 mm vody. Art. U dospělých) je obvykle spojena s hypovolémií v důsledku dehydratace, ztráty krve nebo plazmy. Při výrazném nedostatku bcc v kombinaci se zvýšením objemu vaskulárního lože (anafylaktický šok, blok ganglion) lze pozorovat prudký pokles CVP na minus 50 mm vody. Art.
S rozvojem srdečního selhání je obtížná interpretace dat měření CVP, nicméně v literatuře jsou zprávy o možnosti použití tohoto indikátoru i jako diferenciálního testu.
K posouzení stupně srdečního selhání a BCC můžete použít „expresní index“ navržený G. G. Radzivilem a N. I. Evdokimovem (1976). Autoři pomocí různých hemodynamických parametrů vytvořili vztah mezi obecně dostupnými klinickými indikátory (CVP, srdeční frekvence, krevní tlak), což umožňuje určit poměr mezi objemem cirkulující krve a stupněm srdečního selhání. Tento index je určen vzorcem:
EI \u003d (HR * CVP) / ADsist,
Kde je srdeční frekvence - srdeční frekvence za minutu,
CVP - centrální žilní tlak v mm vody. Art., ADsist. - systolický krevní tlak v mm RT. Art.
Normálně je u zdravých lidí EI 60 - 75;
S hypovolémií se srdečním selháním, EI \u003d 90 - 140;
S "izolovanou" hypovolémií EI \u003d 20 - 25;
Při srdeční slabosti uprostřed normovolémie se EI pohybuje od 150 do 190;
Při srdečním selhání, v kombinaci s hypervolémií, EI dosahuje hodnot 200-300.
Použití navrhovaného indexu pomůže praktickému lékaři při výběru taktiky infuzní terapie.
Je zcela přirozené, že indikátor CVP by měl být interpretován s dalšími laboratorními a funkčními indikátory, klinikou nemoci.
V. A. Chibunovsky (1992) doporučuje, aby byla prováděna kontrolní měření po každém podání 1000 ml tekutiny a že infuzní terapie by měla být zastavena, pokud CVP stoupne nad 120-150 mm vody. Art. Při rychlém zavedení tekutiny se doporučuje kontrolovat CVP po infuzi každých 250 až 500 ml.
Při skutečné hypovolémii Weicker a Ploez (1986) doporučují podání následujících objemů tekutin:
S CVP méně než 30 mm vody. Art. 1-2 l / h;
30 - 100 mm vody. Art. - 1 l / h;
Více než 100 mm vodní sloupec - 0,5 l / h.
II. Zvýrazňující příznaky: vlhkost nebo suchost kůže, dostatek slinění, bronchrhrhea a samozřejmě diuréza.
Renální funkce je na jedné straně indikátorem adekvátnosti infuzní terapie a na druhé straně je selhání ledvin limitujícím bodem, který významně mění taktiku řízení pacienta. Nejčastěji je kritériem přiměřenosti léčby ukazatel normálního hodinového výdeje moči (1 ml / kg za hodinu).
III. Příznaky koncentrace: indikátory Hb, Ht, celkový protein, měrná hmotnost moči.
GU. Nedostatek kliniky intersticiální hyperhydratace: zvýšení tělesné hmotnosti; změny v zrakové nervové jednotce, snížená srdeční frekvence (příznaky mozkového edému); výskyt příznaků plicního edému (sípání ve spodních částech a Rg-obraz stagnace v plicích); periferní edém.

